Перифокальный отек на т2 ви
Если мне нужно сделать фотографию, я достаю из кармана мобильник, выбираю фотоприложение, навожу объектив на понравившийся объект и… щёлк! В 99% случаев я получаю снимок, который сносно отображает необходимый фрагмент реальности.
А ведь ещё несколько десятилетий назад фотографы вручную выставляли выдержку и диафрагму, выбирали фотоплёнку, устраивали проявочную лабораторию в ванной комнате. А снимки получались… ну, такие себе.
Магнитно резонансная томография — потрясающая методика. Для врача, который осознанно управляет параметрами сканирования, она предоставляет огромные возможности в визуализации тканей человеческого организма и патологических процессов.
В зависимости от настроек, одни и те же ткани могут совершенно по разному выглядеть на МР томограммах. Для относительной простоты интерпретации существует несколько более-менее стандартных «режимов» сканирования. Это сделано для того, чтобы МРТ, из категории методик, которыми владеют только одиночки-энтузиасты, пришла в широкую медицинскую практику. Как методика фотографии, которая упростилась настолько, что не только стала доступна каждому, но и порядком успела многим надоесть 😉
Здесь я расскажу о нескольких наиболее часто использующихся режимах сканирования. Поехали!
Т1 ВИ (читается «тэ один вэ и») — режим сканирования, который используется всегда и везде. Свободная безбелковая жидкость (например ликвор в желудочках мозга) на таких изображениях выглядит тёмной, мягкие ткани имеют различные по яркости оттенки серого, а вот жир ярок настолько, что кажется белым. Также на Т1 ВИ очень яркими выглядят парамагнитные контрастные вещества, что и позволяет использовать их для визуализации различных патологических процессов.
Слева — Т1 ВИ, а справа — Т1 ВИ после введения контраста. Опухоль накопила парамагнитный контраст. Просто и красиво!
А ещё на Т1 яркой будет выглядеть гематома на определённых стадиях деградации гемаглобина.
В МРТ «яркий» обозначается термином «гиперинтенсивный»,а «тёмный» — термином «гипоинтенсивный».
Т2 ВИ (читается «тэ два вэ и») — также используется повсеместно. Этот режим наиболее чувствителен к регистрации патологических процессов. Это значит, что большинство патологических очагов, например в головном мозге, будут гиперинтенсивными на Т2 ВИ. А вот определение какой именно патологический процесс мы видим требует применения других режимов сканирования. Помимо патологических процессов и тканей, яркой на Т2 будет свободная жидкость (тот же ликвор в желудочках).
Т2 ВИ — классика в визуализации головного мозга. И вообще, любимая картинка всех МРТшников.
Аббревиатура «ВИ» расшифровывается как «взвешенные изображения». Но боюсь, мне не удастся объяснить смысл этого заклинания без углубления в физику метода.
Pd ВИ (читается «пэ дэ вэ и») — изображения взвешенные по протонной плотности. Что-то среднее между Т1 и Т2 ВИ. Применяется достаточно редко, в связи с появлением более прогрессивных режимов сканирования. Контрастность между разными тканями и жидкостями на таких изображениях довольно низкая. Однако, при исследовании суставов этот режим продолжает пользоваться популярностью, особенно в комплексе с жироподавлением, о котором разговор отдельный.
Слева — Pd ВИ, справа — Т2 ВИ. Одному мне понятно, почему Pd теперь редко используют ?
Словосочетание «режим сканирования» конечно можно использовать, но правильнее использовать словосочетание «импульсная последовательность». Речь про набор радиочастотных и градиентных импульсов, которые используются во время сканирования.
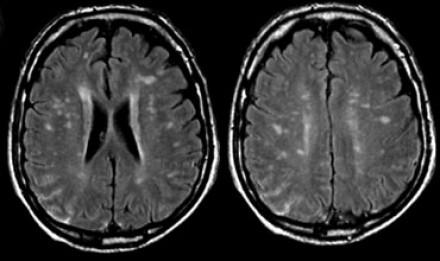
FLAIR (произносится как «флаир» или «флэир») — это Т2 ВИ с ослаблением сигнала от свободной жидкости, например, спинномозговой жидкости. Очень полезная импульсная последовательность, применяется в основном при сканировании головного мозга. На таких изображениях многие патологические очаги видны лучше чем на Т2 ВИ, особенно если они прилежат к пространствам, которые содержат ликвор.
Здесь FLAIR — крайняя картинка справа. Именно на ней лучше всего видны патологические очаги, которые прилежат к желудочкам мозга и субарахноидальному пространству.
Это режимы сканирования или импульсные последовательности, которые наиболее часто используются в ежедневной практике. Но есть ещё много других, которые применяются реже и дают более специфическую информацию.
P.S. Если вам интересно узнать, что такое жиродав и каим он бывает — обязательно поставьте лайк статье, подпишитесь на мой канал в ЯндексДзен или в telegram — так я буду знать, что вы требуете продолжения 😉
Источник
Соавтор: Сотников В. В., к.в.н., главный врач Ветеринарной клиники неврологии, травматологии и интенсивной терапии, г. Санкт-Петербург.
Для выбора оптимальной лечебной тактики и планирования нейрохирургического вмешательства при опухолях головного мозга важно получить наиболее полную диагностическую информацию не только о локализации и гистологических свойствах опухоли, но и о выраженности и характере перифокальных реакций мозга, существенно влияющих на клинические проявления заболевания. Значительный перифокальный отек снижает выживаемость пациентов при менингиомах (Motta L, Mandara MT, Skerritt GC.2012).
Наиболее общей, закономерно развивающейся реакцией при очаговых поражениях (прежде всего при опухолях мозга) является перифокальный отек, в основе развития которого лежит взаимодействие сосудистого и паренхиматозного фактора.
Принято различать вазогенный и цитотоксический отеки мозга, которые могут сочетаться и изменять количественные соотношения в динамике развития в зависимости от вызвавшей их причины. Перифокальный отек при опухолях мозга формируется за счет увеличения объема внеклеточного пространства в результате накопления в нем жидкости, поступающей из поврежденных глиальных клеток, и вследствие повышения проницаемости клеточной мембраны эндотелия капилляров в зоне, окружающей очаг поражения. Распространенность зоны перифокального отека определяется не только увеличением содержания в ней воды, но и степенью регионарной демиелинизации волокон белого вещества мозга.
Чем выше степень демиелинизации, тем меньше содержание липидов в перифокальной зоне и тем более выражены нарушения процессов окисления и фосфорилирования, а также явления отека мозга (Chan Р.Н., Fishmann R.A. 1978). В прогрессировании перифокального отека основную роль играют два механизма: поступление в белое вещество мозга белков плазмы и их связывание с глиальными элементами; увеличение дальнейшего поступления жидкости в перивазальное пространство вследствие осмотического градиента; а также, по аналогичному механизму, поступление жидкости из ликворной системы (Priden F.R., Tsayumu M., Reulen H.J. 1979; S.Reulen H.J., Graber S., Huber P., Jto U. 1988).
Многочисленные исследования в гуманной медицине, проведенные в Институте нейрохирургии АМН Украины, свидетельствуют о существовании динамических различий между явлениями отека и набухания мозга. Отек — это увеличение содержания свободной воды в межклеточных интерстициальных пространствах, а набухание — это накопление свободной воды в клетках и связанной воды в межклеточных пространствах. Для внутримозговых опухолей, особенно для глиом, характерно преобладание отека в перифокальной зоне (О.Ю.Чувашова 2000).
По мере увеличения объема опухоли и нарастания явлений внутричерепной гипертензии изменяется белковый состав как в очаге поражения, так и в перифокальной зоне, в которой эти сдвиги коррелируют со степенью злокачественности опухоли. При этом развиваются регионарные нарушения проницаемости гематоэнцефалического барьера, которые увеличивают цитотоксический отек. Определенную роль в этом процессе, по-видимому, играет обнаруженный недавно в головном мозге специфический белок — фактор проницаемости сосудов, стимулирующий ангиогенез в опухолевой ткани и повышающий проницаемость капилляров, причем обнаружена корреляция между концентрацией этого белка и выраженностью перифокального отека.
Изложенные предпосылки обосновывают поиски возможностей неинвазивного получения диагностической информации, характеризующей выраженность перифокального отека мозга при глиомах с учетом их локализации, величины и гистологических свойств.
По данным МРТ границы глиом и перифокального отека оптимально отличаются в Т2 режиме, поскольку интенсивность сигнала возрастает в зоне большого накопления экстрацеллюлярной жидкости. Рис 1(а)
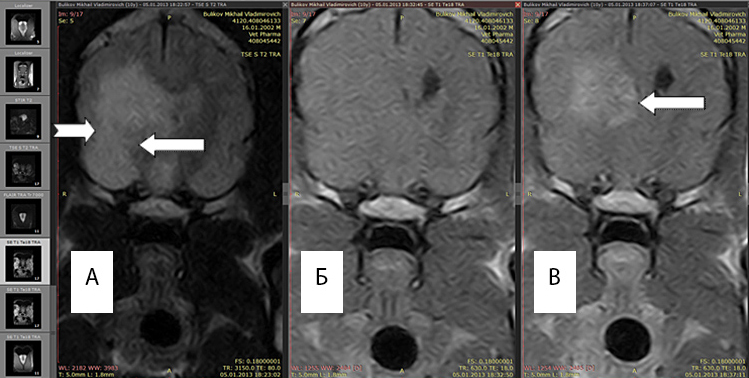 Рис. 1А. Т2 режим, хорошо выражен перифокальный отек (белые стрелки).
Рис. 1А. Т2 режим, хорошо выражен перифокальный отек (белые стрелки).
Рис. 1Б. Т1 режим без введения контраста, отсутствует правый желудочек, имеется смещение срединных структур.
Рис. 1В. Т1 режим с введенным контрастным препаратом «Магневист». Регистрируется интенсивный сигнал от новообразования (обозначено стрелкой), перифокальный отек не виден.
Возможность выявления границ между опухолью и зоной перифокального отека повышается при повторном МРТ-исследовании после введения магнитоусиливающих препаратов (магневист). Поскольку магневист не проникает через неповрежденный гематоэнцефалический барьер, сопоставление томограмм, полученных до и после введения препарата, позволяет судить о регионарных нарушениях проницаемости барьера. Рис 1(A,B)
Это особенно отчетливо проявляется при астроцитомах типичной структуры, при которых функция гематопаренхиматозного барьера на границе опухоли и прилегающих участках мозга до определенного времени остается относительно сохранной, поэтому магневист не проникает в ткань опухоли.
В связи с этим зона гипоинтенсивности сигнала более отчетливо определяется в проекции астроцитомы, чем в области перифокального отека. Оценка размеров и распространения глиом более точна на МРТ, чем на КТ (Кобяков Г.Л., Коновалов А.Н., Личиницер М.Р. 2001; Коновалов A.Н., Корниенко В.Н. 1985; Коновалов А.Н., Корниенко В.Н., Пронин И.Н., 1997.; Yamada K., Soreusen A.G. 2000).
Существует большая точность и разрешающая способность МРТ в диагностике глиом полушарий мозга, этот метод не сопоставим с данными, полученными при КТ-исследовании. Он позволяет более точно определить вид опухоли, степень ее анаплазии и выраженность перифокального отека мозга, что имеет важное значение для выбора наиболее рациональной противоотечной терапии в процессе предоперационной подготовки и планирования хирургического вмешательства (рис. 2,3,4,5,6). На всех рисунках представлены справа результаты МРТ — изображения, а слева — КТ в аналогичных срезах.
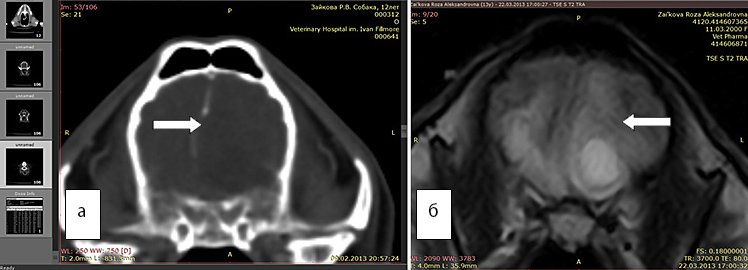 Рис. 2 а. КТ. Заметно смещение срединных структур (стрелка). Отек не виден
Рис. 2 а. КТ. Заметно смещение срединных структур (стрелка). Отек не виден
Рис. 2б. МРТ. Хорошо виден перифокальный отек
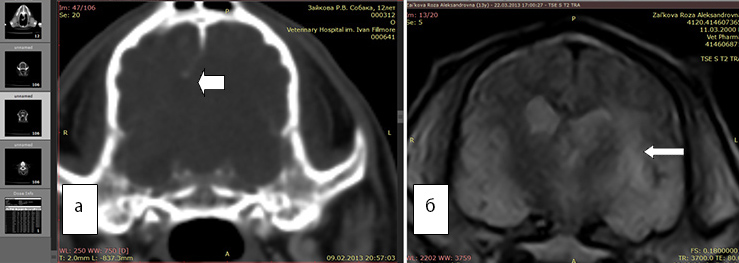 Рис. 3а. КТ. Заметно смещение срединных структур (стрелка). Отек не виден
Рис. 3а. КТ. Заметно смещение срединных структур (стрелка). Отек не виден
Рис. 3б. МРТ. Хорошо виден перифокальный отек
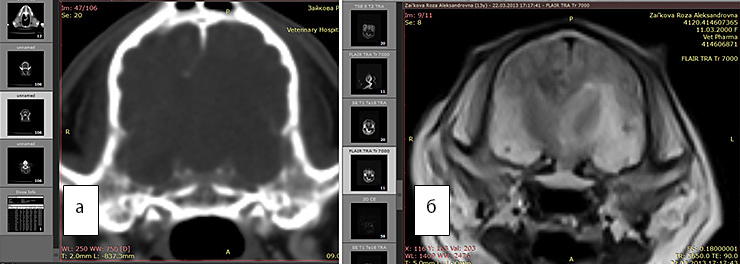 Рис. 4а. КТ. Заметно смещение срединных структур.Отек не виден
Рис. 4а. КТ. Заметно смещение срединных структур.Отек не виден
Рис. 4б. МРТ. Хорошо виден перифокальный отек. FLAIR последовательность
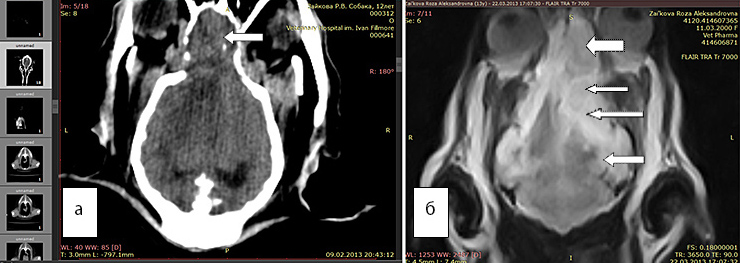 Рис. 5а. КТ. Перифокальный отек плохо виден, но новообразование хорошо заметно (стрелка)
Рис. 5а. КТ. Перифокальный отек плохо виден, но новообразование хорошо заметно (стрелка)
Рис. 5б. МРТ. Видно новообразование (большая стрелка), отек наиболее хорошо виден в программе FLAIR (маленькие стрелки)
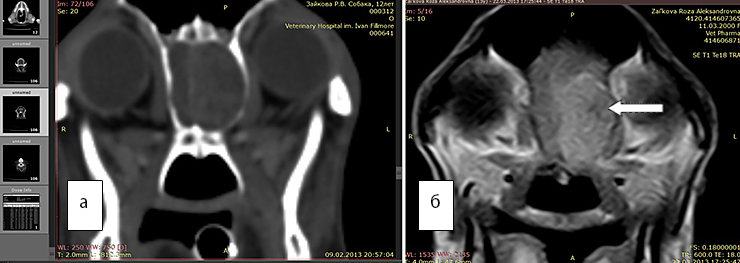 Рис 6а. КТ. В области обонятельной луковицы визуализируется новообразование
Рис 6а. КТ. В области обонятельной луковицы визуализируется новообразование
Рис. 6б. МРТ. Т1 режим с контрастом дает возможность гораздо точнее оценить объем новообразования, его границы
Представленные выше рисунки демонстрируют, что визуализация новообразования головного мозга, перифокального отека и его распространенности гораздо информативнее при использовании МРТ, чем КТ. Улучшить визуализацию помогает использование контраста, а также последовательного выполнения программ: для оценки перифокального отека целесообразно использовать FLAIR импульсную последовательность МРТ. Т2-взвешенные изображения, широко использующиеся для выявления патологических изменений, не всегда позволяют с достаточной надежностью различать зоны поражения и некоторые нормальные ткани. Так, на Т2-взвешенных изображениях зоны патологических изменений вещества мозга часто имеют высокий сигнал и выглядят как более яркие участки. Аналогичный высокий сигнал имеет также нормальная спинномозговая жидкость, что затрудняет выявление патологических очагов, располагающихся около пространств, заполненных данной жидкостью. Для преодоления данного недостатка разработана методика FLAIR (Fluid Attenuated Inversion Recovery), обеспечивающая подавление сигнала свободной воды (спинномозговой и некоторых других физиологических жидкостей) при сохранении базовой Т2-взвешенности изображения. FLAIR лучше выявляет очаговые изменения мозга.
Нельзя не отметить, что (по нашим данным наблюдения 35 пациентов) оценить наличие и размер перифокального отека при ЭЭГ — исследовании невозможно. Такая же ситуация существует и в гуманной медицине. Изменения биоэлектрической активности мозга (ЭЭГ) при глиальных опухолях неспецифичны и отражают реакцию мозга на поражение, развивающееся в нем. В дооперационном периоде ЭЭГ позволяет получить объективную информацию о функциональном состоянии мозга, выявить наличие и локализацию эпилептического очага у пациентов, имеющих эпилептические припадки (Фадеева Т.Н. 2004). Следует исходить из данных о том, что опухолевая ткань электрически нейтральна, поэтому на ЭЭГ нет отражения места локализации опухоли. Однако при проведении противоотечной терапии (дексаметазон 1мг/кг 2 раза в день) перед оперативным лечением либо при неоперабельных опухолях вместе с регрессом неврологических симптомов очень быстро происходит нормализация электрической активности головного мозга, что, несомненно, указывает на влияние перифокального отека на электрическую активность мозга.
Список литературы:
- Chan Р.Н., Fishmann R.A. Brain edema: induction in cortical slices by polyunsaturated fatty acids //Science. — 1978. — V.201, №5607. — P.358—360.
- Priden F.R., Tsayumu M., Reulen H.J. Measurement of vasogenic brain edema clearance into ventricular CSF //Surg. Forum. — 1979. — V.30, №5. — P. 446—453.
- S.Reulen H.J., Graber S., Huber P., Jto U. Factors off ecting the extension of peritumoral brain oedema ACT-study //Acta Neurochir. — 1988. — V.96, №1—2. — P. 19—24.
- Motta L., Mandara M. T., Skerritt G. C. Canine and feline intracranial meningiomas: an updated review. The Veterinary Journal, 192, 153-165. Source ChesterGates Animal Referral Hospital, Chester Gate Road, Telford Court, Unit E-F, Chester CH16LT, United Kingdom.
- Чувашова О.Ю. Характеристика перифокального отека при глиомах полушарий головного мозга различной степени анаплазии по данным компьютерной и магнитно-резонансной томографии. Институт нейрохирургии им. акад. А.П.Ромоданова АМН Украины, г. Киев. 2000.
- Кобяков Г.Л., Коновалов А.Н., Личиницер М.Р. и др. Современные возможности химиотерапии в лечении злокачественных опухолей // Современные минимально-инвазивные технологии (нейрохирургия, вертебрология, неврология, нейрофизиология): Материалы симпозиума. — СПб., 2001.—С. 251-253.
- Коновалов A.Н., Корниенко В.Н. Компьютерная томография в нейрохирургической клинике. — М.: Медицина, 1985.— С. 20—44.
- Коновалов А.Н., Корниенко В.Н., Пронин И.Н. Магнитно-резонансная томография в нейрохирургии. — М.: Видар, 1997.—С. 95-134.
- Yamada K., Soreusen A.G. Diagnostic imaging // Neurooncology. The Essentials. — New York, 2000. — Ch. 6. — P. 56 —77
Источник
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА ПОРАЖЕНИЙ БЕЛОГО ВЕЩЕСТВА
Дифференциально-диагностический ряд заболеваний белого вещества является очень длинным. Выявленные с помощью МРТ очаги могут отражать нормальные возрастные изменения, но большинство очагов в белом веществе возникают в течение жизни и в результате гипоксии и ишемии.
Рассеянный склероз считается самым распространенным воспалительным заболеванием, которое характеризуется поражением белого вещества головного мозга. Наиболее частыми вирусными заболеваниями, приводящими к возникновению похожих очагов, являются прогрессирующая мультифокальная лейкоэнцефалопатия и герпесвирусная инфекция. Они характеризуются симметричными патологическими участками, которые нужно дифференцировать с интоксикациями.
Сложность дифференциальной диагностики обусловливает в ряде случаев необходимость дополнительной консультации с нейрорадиологом с целью получения второго мнения.
ПРИ КАКИХ БОЛЕЗНЯХ ВОЗНИКАЮТ ОЧАГИ В БЕЛОМ ВЕЩЕСТВЕ?
Очаговые изменения сосудистого генеза
- Атеросклероз
- Гипергомоцистеинемия
- Амилоидная ангиопатия
- Диабетическая микроангиопатия
- Гипертония
- Мигрень
Воспалительные заболевания
- Рассеянный склероз
- Васкулиты: системная красная волчанка, болезнь Бехчета, болезнь Шегрена
- Саркоидоз
- Воспалительные заболевания кишечника (болезнь Крона, язвенный колит, целиакия)
Заболевания инфекционной природы
- ВИЧ, сифилис, боррелиоз (болезнь Лайма)
- Прогрессирующая мультифокальная лейконцефалопатия
- Острый рассеянный (диссеминированный) энцефаломиелит (ОДЭМ)
Интоксикации и метаболические расстройства
- Отравление угарным газом, дефицит витамина B12
- Центральный понтинный миелинолиз
Травматические процессы
- Связанные с лучевой терапией
- Постконтузионные очаги
Врожденные заболевания
- Обусловленные нарушением метаболизма (имеют симметричный характер, требуют дифференциальной диагностики с токсическими энцефалопатиями)
Могут наблюдаться в норме
- Перивентрикулярный лейкоареоз, 1 степень по шкале Fazekas
МРТ ГОЛОВНОГО МОЗГА: МНОЖЕСТВЕННЫЕ ОЧАГОВЫЕ ИЗМЕНЕНИЯ
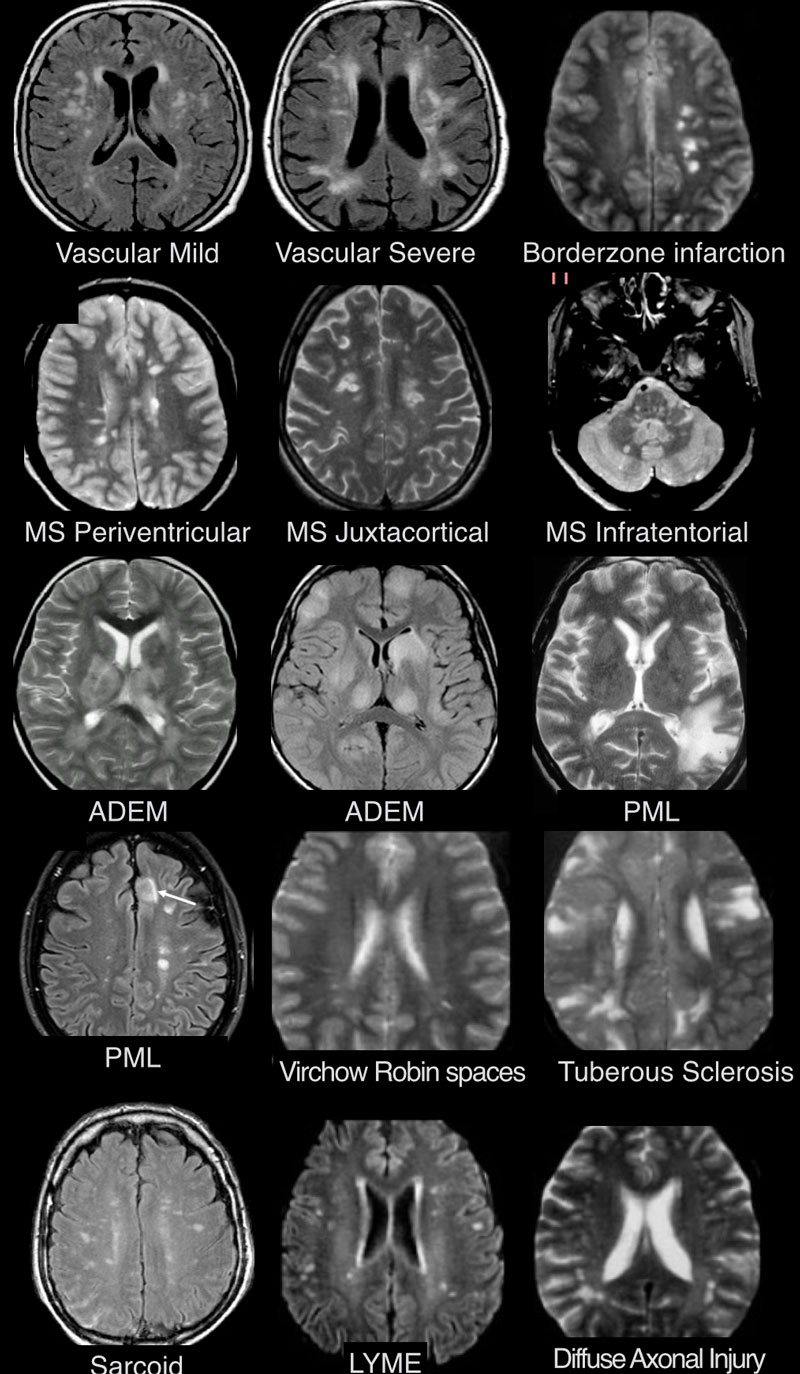
На изображениях определяются множественные точечные и «пятнистые» очаги. Некоторые из них будут рассмотрены более детально.
Инфаркты по типу водораздела
- Главное отличие инфарктов (инсультов) этого типа — это предрасположенность к локализации очагов только в одном полушарии на границе крупных бассейнов кровоснабжения. На МР-томограмме представлен инфаркт в бассейне глубоких ветвей.
Острий диссеминированный энцефаломиелит (ОДЭМ)
- Основное отличие: появление мультифокальных участков в белом веществе и в области базальных ганглиев через 10-14 дней после перенесенной инфекции или вакцинации. Как при рассеянном склерозе, при ОДЭМ может поражаться спинной мозг, дугообразные волокна и мозолистое тело; в некоторых случаях очаги могут накапливать контраст. Отличием от РС считается тот момент, что они имеют большой размер и возникают преимущественно у молодых пациентов. Заболевание отличается монофазным течением
Болезнь Лайма
- Характеризуется наличием мелких очажков размером 2-3 мм, имитирующих таковые при РС, у пациента с кожной сыпью и гриппоподобным синдромом. Другими особенностями являются гиперинтенсивный сигнал от спинного мозга и контрастное усиление в области корневой зоны седьмой пары черепно-мозговых нервов.
Саркоидоз головного мозга
- Распределение очаговых изменений при саркоидозе крайне напоминает таковое при рассеянном склерозе.
Прогрессирующая мультфокальная лейкоэнцефалопатия (ПМЛ)
- Демиелинизирующее заболевание, обусловленное вирусом Джона Каннигема у пациентов с иммунодефицитом. Ключевым признаком являются поражения белого вещества в области дугообразных волокон, не усиливающиеся при контрастировании, оказывающие объемное воздействие (в отличие от поражений, обусловленных ВИЧ или цитомегаловирусом). Патологические участки при ПМЛ могут быть односторонними, но чаще они возникают с обеих сторон и являются асимметричными.
Пространства Вирхова-Робина
- Ключевой признак: гиперинтенсивный сигнал на Т2 ВИ и гипоинтенсивный на FLAIR
Сосудистые очаги
- Для зон сосудистого характера типична глубокая локализация в белом веществе, отсутствие вовлечения мозолистого тела, а также юкставентрикулярных и юкстакортикальных участков.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА МНОЖЕСТВЕННЫХ ОЧАГОВ, УСИЛИВАЮЩИХСЯ ПРИ КОНТРАСТИРОВАНИИ
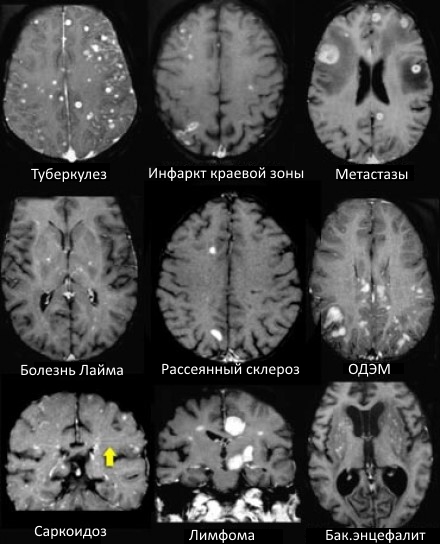
На МР-томограммах продемонстрированы множественные патологические зоны, накапливающие контрастное вещество. Некоторые из них описаны далее подробнее.
Васкулиты
- Большинство васкулитов характеризуются возникновением точечных очаговых изменений, усиливающихся при контрастировании. Поражение сосудов головного мозга наблюдается при системной красной волчанке, паранеопластическом лимбическом энцефалите, б. Бехчета, сифилисе, гранулематозе Вегенера, б. Шегрена, а также при первичных ангиитах ЦНС.
Болезнь Бехчета
- Чаще возникает у пациентов турецкого происхождения. Типичным проявлением этого заболевания признано вовлечение мозгового ствола с появлением патологических участков, усиливающихся при контрастировании в острой фазе.
Метастазы
- Характеризуются выраженным перифокальным отеком.
Инфаркт по типу водораздела
- Периферические инфаркты краевой зоны могут усиливаться при контрастировании на ранней стадии.
ПЕРИВАСКУЛЯРНЫЕ ПРОСТРАНСТВА ВИРХОВА-РОБИНА
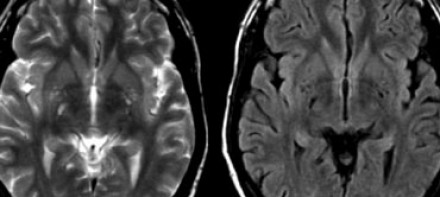
Слева на Т2-взвешенной томограмме видны множественные очаги высокой интенсивности в области базальных ганглиев. Справа в режиме FLAIR сигнал от них подавляется, и они выглядят темными. На всех остальных последовательностях они характеризуются такими же характеристиками сигнала, как ликвор (в частности, гипоинтенсивным сигналом на Т1 ВИ). Такая интенсивность сигнала в сочетании с локализацией описанного процесса являются типичными признаками пространств Вирхова-Робина (они же криблюры).
Пространства Вирхова-Робина окружают пенетрирующие лептоменингеальные сосуды, содержат ликвор. Их типичной локализацией считается область базальных ганглиев, характерно также расположение вблизи передней комиссуры и в центре мозгового ствола. На МРТ сигнал от пространств Вирхова-Робина на всех последовательностях аналогичен сигналу от ликвора. В режиме FLAIR и на томограммах, взвешенных по протонной плотности, они дают гипоинтенсивный сигнал в отличие от очагов иного характера. Пространства Вирхова-Робина имеют небольшие размеры, за исключением передней комиссуры, где периваскулярные пространства могут быть больше.
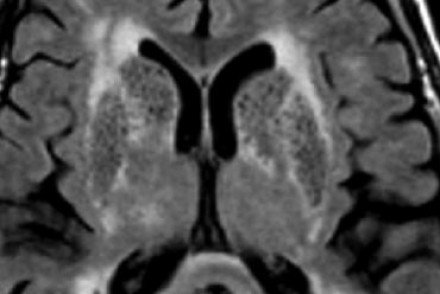
На МР-томограмме можно обнаружить как расширенные периваскулярные пространства Вирхова-Робина, так и диффузные гиперинтенсивные участки в белом веществе. Данная МР-томограмма превосходно иллюстрирует различия между пространствами Вирхова-Робина и поражениями белого вещества. В данном случае изменения выражены в значительной степени; для их описания иногда используется термин «ситовидное состояние» (etat crible). Пространства Вирхова-Робина увеличиваются с возрастом, а также при гипертонической болезни в результате атрофического процесса в окружающей ткани мозга.
НОРМАЛЬНЫЕ ВОЗРАСТНЫЕ ИЗМЕНЕНИЯ БЕЛОГО ВЕЩЕСТВА НА МРТ
К ожидаемым возрастным изменениям относятся:
- Перивентрикулярные «шапочки» и «полосы»
- Умеренно выраженная атрофия с расширением борозд и желудочков мозга
- Точечные (и иногда даже диффузные) нарушения нормального сигнала от мозговой ткани в глубоких отделах белого вещества (1-й и 2-й степени по шкале Fazekas)
Перивентрикулярные «шапочки» представляют собой области, дающие гиперинтенсивный сигнал, расположенные вокруг передних и задних рогов боковых желудочков, обусловленные побледнением миелина и расширением периваскулярных пространств. Перивентрикулярные «полосы» или «ободки» это тонкие участки линейной формы, расположенные параллельно телам боковых желудочков, обусловленные субэпендимальным глиозом.
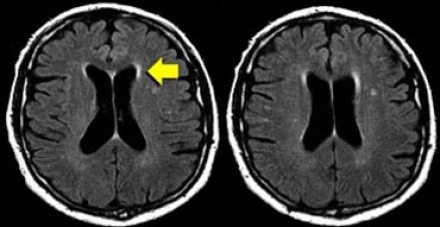
На магнитно-резонансных томограммах продемонстрирована нормальная возрастная картина: расширение борозд, перивентрикулярные «шапочки» (желтая стрелка), «полосы» и точечные очажки в глубоком белом веществе.
Клиническое значение возрастных изменений мозга недостаточно хорошо освещено. Тем не менее, имеется связь между очагами и некоторыми факторами риска возникновения цереброваскулярных расстройств. Одним из самых значительных факторов риска является гипертония, особенно, у пожилых людей.
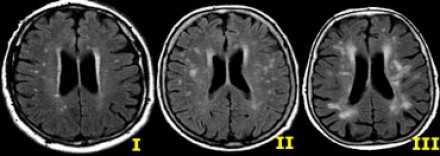
Степень вовлечения белого вещества в соответствии со шкалой Fazekas:
- Легкая степень – точечные участки, Fazekas 1
- Средняя степень – сливные участки, Fazekas 2 (изменения со стороны глубокого белого вещества могут расцениваться как возрастная норма)
- Тяжелая степень – выраженные сливные участки, Fazekas 3 (всегда являются патологическими)
ДИСЦИРКУЛЯТОРНАЯ ЭНЦЕФАЛОПАТИЯ НА МРТ
Очаговые изменения белого вещества сосудистого генеза — самая частая МРТ-находка у пациентов пожилого возраста. Они возникают в связи с нарушениями циркуляции крови по мелким сосудам, что является причиной хронических гипоксических/дистрофических процессов в мозговой ткани.
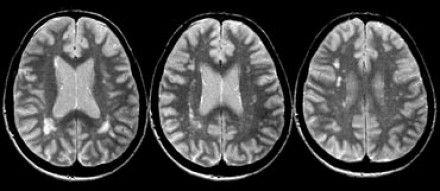
На серии МР-томограмм: множественные гиперинтенсивные участки в белом веществе головного мозга у пациента, страдающего гипертонической болезнью.
На МР-томограммах, представленных выше, визуализируются нарушения МР-сигнала в глубоких отделах больших полушарий. Важно отметить, что они не являются юкставентрикулярными, юкстакортикальными и не локализуются в области мозолистого тела. В отличие от рассеянного склероза, они не затрагивают желудочки мозга или кору. Учитывая, что вероятность развития гипоксически-ишемических поражений априори выше, можно сделать заключение о том, что представленные очаги, вероятнее, имеют сосудистое происхождение.
Только при наличии клинической симптоматики, непосредственно указывающей на воспалительное, инфекционное или иное заболевание, а также токсическую энцефалопатию, становится возможным рассматривать очаговые изменения белого вещества в связи с этими состояниями. Подозрение на рассеянный склероз у пациента с подобными нарушениями на МРТ, но без клинических признаков, признается необоснованным.
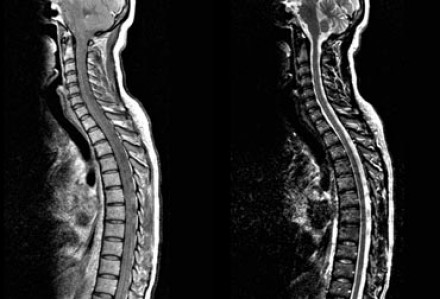
На представленных МР-томограммах патологических участков в спинном мозге не выявлено. У пациентов, страдающих васкулитами или ишемическими заболеваниями, спинной мозг обычно не изменен, в то время как у пациентов с рассеянным склерозом в более чем 90% случаев обнаруживаются патологические нарушения в спинном мозге. Если дифференциальная диагностика очагов сосудистого характера и рассеянного склероза затруднительна, например, у пожилых пациентов с подозрением на РС, может быть полезна МРТ спинного мозга.
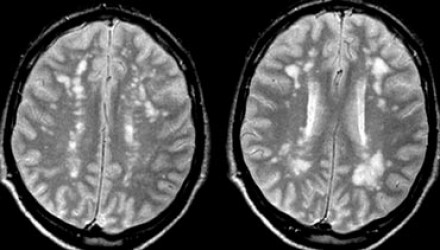
Вернемся снова к первому случаю: на МР-томограммах выявлены очаговые изменения, и сейчас они гораздо более очевидны. Имеет место распространенное вовлечение глубоких отделов полушарий, однако дугообразные волокна и мозолистое тело остаются интактными. Нарушения ишемического характера в белом веществе могут проявляться как лакунарные инфаркты, инфаркты пограничной зоны или диффузные гиперинтенсивные зоны в глубоком белом веществе.
Лакунарные инфаркты возникают в результате склероза артериол или мелких пенетерирующих медуллярных артерий. Инфаркты пограничной зоны возникают в результате атеросклероза более крупных сосудов, например, при каротидной обструкции или вследствие гипоперфузии.
Структурные нарушения артерий головного мозга по типу атеросклероза наблюдаются у 50% пациентов старше 50 лет. Они также могут обнаруживаться и у пациентов с нормальным артериальным давлением, однако более характерны для гипертоников.
САРКОИДОЗ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ

Распределение патологических участков на представленных МР-томограммах крайне напоминает рассеянный склероз. Помимо вовлечения глубокого белого вещества визуализируются юкстакортикальные очаги и даже «пальцы Доусона». В итоге было сделано заключение о саркоидозе. Саркоидоз не зря называют «великим имитатором», т. к. он превосходит даже нейросифилис по способности симулировать проявления других заболеваний.
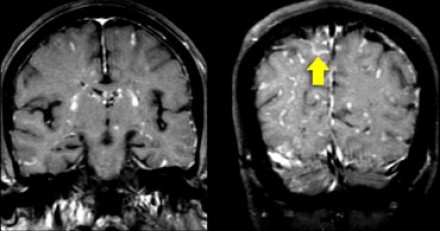
На Т1 взвешенных томограммах с контрастным усилением препаратами гадолиния, выполненных этому же пациенту, что и в предыдущем случае, визуализируются точечные участки накопления контраста в базальных ядрах. Подобные участки наблюдаются при саркоидозе, а также могут быть обнаружены при системной красной волчанке и других васкулитах. Типичным для саркоидоза в этом случае считается лептоменингеальное контрастное усиление (желтая стрелка), которое происходит в результате гранулематозного воспаления мягкой и паутинной оболочки.
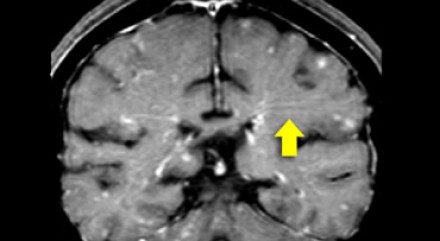
Еще одним типичным проявлением в этом же случае является линейное контрастное усиление (желтая стрелка). Оно возникает в результате воспаления вокруг пространств Вирхова-Робина, а также считается одной из форм лептоменингеального контрастного усиления. Таким образом объясняется, почему при саркоидозе патологические зоны имеют схожее распределение с рассеянным склерозом: в пространствах Вирхова-Робина проходят мелкие пенетрирующие вены, которые поражаются при РС.
БОЛЕЗНЬ ЛАЙМА (БОРРЕЛИОЗ)
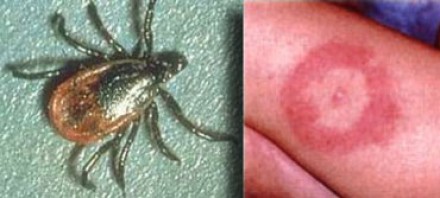
На фотографии справа: типичный вид сыпи на коже, возникающей при укусе клеща (слева) — переносчика спирохет.
Болезнь Лайма, или боррелиоз, вызывают спирохеты (Borrelia Burgdorferi), переносчиком инфекции являются клещи, заражение происходит трансмиссивным путем (при присасывании клеща). В первую очередь при боррелиозе на возникает кожная сыпь. Через несколько месяцев спирохеты могут инфицировать ЦНС, в результате чего появляются патологические участки в белом веществе, напоминающие таковые при рассеянном склерозе. Клинически болезнь Лайма проявляется острой симптоматикой со стороны ЦНС (в том числе, парезами и параличами), а в некоторых случаях может возникать поперечный миелит.
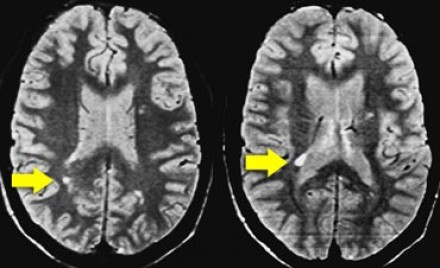
Ключевой признак болезни Лайма — это наличие мелких очажков размером 2-3 мм, симулирующих картину рассеянного склероза, у пациента с кожной сыпью и гриппоподобным синдромом. К другим признакам относится гиперинтенсивный сигнал от спинного мозга и контрастное усиление седьмой пары черепно-мозговых нервов (корневая входная зона).
ПРОГРЕССИРУЮЩАЯ МУЛЬТИФОКАЛЬНАЯ ЛЕЙКОЭНЦЕФАЛОПАТИЯ, ОБУСЛОВЛЕННАЯ ПРИЕМОМ НАТАЛИЗУМАБА
Прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ) является демиелинизирующим заболеванием, обусловленным вирусом Джона Каннингема у пациентов с иммунодефицитом. Натализумаб представляет собой препарат моноклоанальных антител к интегрину альфа-4, одобренный для лечения рассеянного склероза, т. к. он оказывает положительный эффект клинически и при МРТ исследованиях.
Относительно редкий, но в то же время серьезный побочный эффект приема этого препарата — повышение риска развития ПМЛ. Диагноз ПМЛ основывается на клинических проявлениях, обнаружении ДНК вируса в ЦНС (в частности, в цереброспинальной жидкости), и на данных методов визуализации, в частности, МРТ.
По сравнению с пациентами, у которых ПМЛ обусловлен другими причинами, например, ВИЧ, изменения на МРТ при ПМЛ, связанной с приемом натализумаба, могут быть описаны как однородные и с наличием флю?
