Онкотическое давление крови отеки
Онкотическое давление (от др.-греч. ὄγκος — объем, масса) — коллоидно-осмотическое давление, доля осмотического давления, создаваемая высокомолекулярными компонентами раствора. В плазме крови человека составляет лишь около 0,5 % осмотического давления (3—4 кн/м², или 0,03—0,04 атм). Тем не менее онкотическое давление играет важнейшую роль в образовании межклеточной жидкости, первичной мочи и др. Стенка капилляров свободно проницаема для воды и низкомолекулярных веществ, но не для белков. Скорость фильтрации жидкости через стенку капилляра определяется разницей между онкотическим давлением белков плазмы и гидростатическим давлением крови, создаваемым работой сердца. На артериальном конце капилляра солевой раствор вместе с питательными веществами переходит в межклеточное пространство. На венозном конце капилляра процесс идёт в противоположном направлении, поскольку венозное давление ниже онкотического давления. В результате в кровь переходят вещества, отдаваемые клетками. При заболеваниях, сопровождающихся уменьшением концентрации в крови белков (особенно альбуминов), онкотическое давление снижается, и это может явиться одной из причин накопления жидкости в межклеточном пространстве, в результате чего развиваются отёки.
В биологии[править | править код]
Кровь, лимфа, а также все тканные жидкости живых организмов являются водными растворами органических и минеральных соединений, и ионов. Им свойственно определенное осмотическое давление. Осмотическое давление крови человека достаточно постоянно, при 309,75К оно достигает 0,74-0,78 МПа. Ему соответствует осмолярная концентрация растворенных в плазме веществ, которая составляет 0,287-0,0303 кг/м3. Осмотическое давление крови обуславливает растворенная в ней небольшая часть ионов. Высокомолекулярные соединения, зачастую белки (альбумины, глобулины), составляют половину процента общего давления крови. Эту часть осмотического давления называют онкотическим давлением, величина которого достигает 3,5-3,9 кПа. Постоянность осмотического давления в крови регулируется выделением паров воды при дыхании, работой почек, выделением пота и т.д.
Онкотическое давление имеет важное значение для жизнедеятельности организма. Понижение содержания белка в крови (гипопротеиномия, голодание, нарушение деятельности пищеварительного тракта, потеря белка с мочой при заболевании почек) вызывает разницу в онкотическом давлении в тканных жидкостях и крови. Вода стремится в сторону большего давления (в ткани); возникают так называемые онкотические отеки подкожной клетчатки («голодные» и «почечные» отеки). При оценке состояния и лечении больных учет осмоонкотических явлений имеет огромное значение.
Организм человека способен поддерживать осмотическое давление на постоянном уровне. При его изменении организм стремится вернуть его в норму. Так, если с едой в организм вводится большое количество растворенных веществ (соль, сахар), осмотическое давление изменится, на что организм сразу же отреагирует: меняется количество и состав слюны, пота, мочи и количество выделительной пары. На рецепторы языка подается сигнал жажды. Человек начинает пить воду, снижая осмотическое давление.
При патологических явлениях в тканях организма осмотическое давление может значительно колебаться и в центре воспаления оно превышает норму в два-три раза.
Растворы с осмотическим давлением, которое равно давлению раствора, принятого за стандарт, называют изотоническими. Растворы с осмотическим давлением, высшим за стандарт, называют гипертоническими, а низшим — гипотоническими.
В медицинской практике изотоническими растворами называют растворы с осмотическим давлением, которое равно осмотическому давлению плазмы крови. Таким раствором является 0,85%-ный раствор хлорида натрия (146 моль/м3). В таком очень разведенном растворе NaCl изотонический коэффициент Вант-Гоффа можно считать равным 2, и рассчитанное значение осмотического давления для этих растворов при 310К (или ) будет равно:
МПа.
Изотоническим относительно плазмы крови является также 4,5-5%-ный раствор глюкозы.
Изотонические растворы можно вводить в организм человека в больших количествах. Такие растворы вводят больным по несколько литров в сутки, например, после тяжелых операций для компенсации потерь крови.
Гипертонические растворы вводят в организм человека только в небольших кол-вах. При введении большого количества гипертонического раствора эритроциты вследствие экзоосмоса теряют воду, резко уменьшаются в объеме и сморщиваются (плазмолиз).
В хирургии гипертонические растворы применяют как внешнее для смачивания марлевых повязок, которые используются при лечении гнойных ран. Если ребенок, например, повредил колено и рана начала гноится, хорошо было бы сделать такую перевязку. Ибо согласно с законом осмоса жидкость с раны стремится по марле наружу, что способствует очищению раны от гноя, микроорганизмов, продуктов распада и т.д.
Гипертонические растворы некоторых солей (), которые плохо всасываются желудочно-кишечным трактом, используют как средства для поноса. Слабительное действие солей связано с тем, что вследствие осмоса осуществляется переход большого количества воды со слизистой оболочки в кишечник.
Во всех случаях, когда с определенными терапевтическими намерениями в кровяное русло, мышечную ткань, спинномозговой канал и т.д. вводят солевые растворы (физиологические растворы), необходимо проводить такую операцию очень тщательно, чтобы не вызвать «осмотического конфликта» — несоответствия между осмотическим давлением плазмы крови, межклеточной или спинномозговой жидкостью и осмотическим давлением раствора, который вливается. Если, например, тот раствор, который вводится, будет гипертоническим по отношению к крови, то при этом будет осуществляться осмос воды из внутренних частей эритроцитов в окружающую плазму, эритроциты будут обезвоживаться и сморщиваться. Если же раствор, который вводится, будет гипотоническим по отношению к крови, то осмос будет осуществляться в обратном направлении — внутрь эритроцитов (эндоосмос). Эритроциты при этом будут увеличиваться в объеме, что может привести к разрыву их оболочки и деструкции (настает гемолиз). Начальная стадия гемолиза настает при снижении осмотического давления в плазме от 0,40-0,36 МПа, а полный гемолиз — при 0,26-0,30 МПа.
Гемолиз является отдельным случаем общего явления — цитолиза — разрушения животных и растительных клеток под влиянием разницы осмотических давлений по разные стороны мембраны клетки. Опасные последствия гемолиза можно уменьшить путём снижения проницаемости клеточной оболочки, что достигается введением строфантина, гепарина и других препаратов.
Осмос и диализ лежат в основе целого ряда физиологических процессов, которые протекают в организме человека и животных. С их помощью осуществляется усвоение еды, окислительные процессы, связанные с дыханием, распределение нутриентов, которые переносятся кровью, и жидкостный обмен в тканях, выделение продуктов жизнедеятельности (мочи, кала) и т.д. Используя слишком соленую или сладкую еду, человек чувствует жажду, которая дает сигнал про возрастание в клетках и межклеточных жидкостях осмотического давления. При купании в морской воде отмечается покраснение глаз с незначительными болями, поскольку под действием осмоса вода с глаза высасывается в морскую воду, где выше осмотическое давление, и глаз будто частично высыхает. При купании в пресной воде болевые ощущения, резь в глазах более ощутимы, потому что осмос воды направленный внутрь глаза.
Неравномерное распределение ионов в живых мембранах вызывает появление электрических потенциалов, которые имеют большое значение в физиологии. Способность некоторых мембран концентрировать ионы впечатляющая. Например, в носовых солевых железах альбатроса, буревестника и некоторых других морских птиц содержатся мембраны, которые осуществляют транспортирование хлористого натра с внутренних клеток на поверхность желез в таких высоких концентрациях, что с кончика птичьего клюва капает 5%-ный раствор соли. Специальная адаптация позволяет птицам пить морскую воду и выживать в среде, где нет пресной воды.
См. также[править | править код]
- Кровообращение
Источник
Отеки вследствие повышенного гидростатического давления. Отеки вследствие пониженного онкотического давления.
Характерным признаком является зависимость от положения тела; венозный застой в соответствующей области (клинически выявляется не всегда); изменений в сыворотке крови нет.
Отек такого типа наиболее часто находят при местно обусловленном застое вследствие перенесенного тромбофлебита и варикозного расширения вен (варикозный симптомокомплекс). Такие случаи очень часты. В анамнезе, как правило, отмечается флебит. Отеки располагаются на голенях, в большинстве случаев несимметрично, часто только на одной конечности. В таких случаях на пораженной конечности имеются изменения вен (расширение вен или завершившийся тромботический процесс), что обычно не трудно распознать. На коже голеней часты пигментация и изъязвления.
Нередко эти случаи осложняются присоединившейся сердечной недостаточностью.
Кроме застоя вследствие поражения вен, застойные отеки могут иметь место также при сдавлении вен малого таза: у женщин — при гинекологических заболеваниях, у мужчин — при раке предстательной железы. Причиной отека нижних конечностей часто являются также нарушения в системе воротной вены и циррозы печени.
Значительно менее определенно удается связать исключительно с повышенным гидростатическим давлением в капиллярах отек при гемодинамической сердечной недостаточности, хотя некоторые особенности сердечных отеков, и прежде всего их выраженная зависимость от положения тела (преимущественно на голенях у ходячих больных и в поясничной области у лежачих), указывают на важность гидростатического фактор а. Однако в последнее время подчеркивается, что существенное значение в генезе сердечных отеков имеет также недостаточное выделение хлористого натрия вследствие уменьшения почечного кровотока при уменьшенном выбросе сердца (forward failure). Еще важнее гиперпродукция альдостерона, которая при возникновении отеков наступает, очевидно, как вторичное явление и поддерживает образование последних тем, что уменьшает выделение натрия. В далеко зашедших случаях, сопровождающихся застоем печени, когда развивается печеночная недостаточность с гипопротеинемией, определенную роль играет также фактор уменьшения онкотического давления.
Для диагноза сердечного отека решающим является выявление наличия гемодинамической сердечной недостаточности.
При ожирении, даже и без явлений сердечной недостаточности, условия оттока настолько нарушаются, что могут образовываться гидростатические отеки.
Наследственный хронический отек типа Нонне — Мейге — Милрой (Nonne—Meige—Milroу) — редкое заболевание, главную роль в возникновении которого, вероятно, играет неполноценность вен или лимфатических сосудов. Ясные симптомы появляются большей частью в период полового созревания; на продолжительность жизни они не влияют. Одинаково поражаются оба пола.
Отеки вследствие пониженного онкотического давления. Характерные признаки: малая зависимость от положения тела, низкое содержание белка в сыворотке крови.
Прототипом этой группы является отек при нефрозе, который идет параллельно с очень низким содержанием сывороточного белка. Решающий диагностический критерий — гипопротеинемия. Клинически нефротические отеки отличаются сравнительной независимостью от положения тела; они, следовательно, располагаются не только на нижних конечностях, но прежде всего также на лице, преимущественно на веках. Обычно эти отеки сопровождаются значительной протеинуриеи, которая и является путеводной нитью в распознавании болезни.
Тяжелые заболевания печени протекают, как правило, с отеками (от умеренных до распространенных), обусловленными гипопротеинемией, которая в свою очередь вызвана недостаточным образованием белка в печени. К правильному диагнозу приводят другие симптомы печеночной недостаточности.
Голодные отеки в основе своей имеют гипопротеинемию, хотя повинны и другие факторы (повреждение капилляров?). Голодные отеки возникают и при однообразной, бедной белком пище не только во времена подлинно всеобщих бедствий, что всегда надо выяснять соответствующим расспросом относительно условий питания.
В основе тяжелых кахектических состояний (туберкулез» опухоли и т. д.) лежат те же причины. Как и при голодных отеках, выделение белка с мочой также и в этих случаях отступает на задний план.
К этой же группе относятся отеки при тяжелых ожогах, бери-бери и хроническом алкоголизме.
При всех неясных гипопротеинемических состояниях надо всегда искать лежащее в основе первичное заболевание.
— Также рекомендуем «Отеки вследствие нарушения обмена электролитов. Отеки вследствие нарушения капиллярной стенки.»
Оглавление темы «Болезни почек. Отеки и их причины.»:
1. Оценка почечной функции. Проба с фенолсульфофталеином.
2. Клиника уремии. Признаки уремии. Псевдоуремия.
3. Гепато-ренальный синдром. Экстраренальный почечный синдром.
4. Злокачественные опухоли почек. Саркома почек.
5. Нефролитиаз. Почечная колика.
6. Гидронефроз. Пиелонефрит. Признаки гидронефроза и пиелонефрита.
7. Пионефроз. Протеинурия. Признаки и классификация протеинурии.
8. Отеки. Причины отеков. Воспалительный отек.
9. Отеки вследствие повышенного гидростатического давления. Отеки вследствие пониженного онкотического давления.
10. Отеки вследствие нарушения обмена электролитов. Отеки вследствие нарушения капиллярной стенки.
Источник
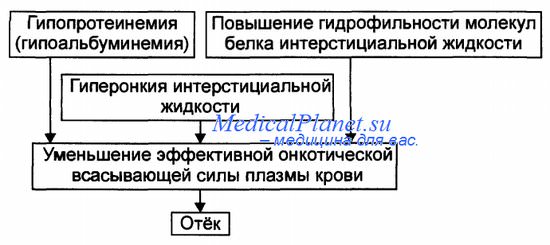
Для онкотического (гипоальбуминемического, гипопротеинемического) фактора развития отёка характерно снижение онкотического давления крови и/или увеличение его в межклеточной жидкости.-
• Причины включения онкотического фактора представлены на рисунке.
— Снижающие онкотическое давление крови в результате гипопротеинемии. Гипопротеинемия (в основном за счёт гипоальбуминемии; альбумины примерно в 2,5 раза более гидрофильны, чем глобулины) наиболее часто является следствием:
— Недостаточности поступления белков в организм при:
— общем или белковом голодании;
— нарушении полостного и/или мембранного пищеварения (например, при резекции фрагментов кишечника, дисбактериозе, синдромах мальабсорбции).
— Снижения синтеза альбуминов в печени (например, при воздействии на неё гепатотропных ядов, выраженном циррозе).
— Избыточной потери белка организмом (например, с мочой при нефротическом синдроме, с плазмой крови при обширных ожогах, с калом при расстройстве пищеварения в желудке и кишечнике).

Причины включения онкотического фактора развития отёка
Вышеназванные факторы вызывают снижение содержания альбуминов.
— Повышающие онкотическое давление интерстициальной жидкости. Эти причины имеют в основном регионарное значение и вызывают или потенцируют развитие местных отёков. Гиперонкия интерстициальной жидкости является результатом:
— Избыточного транспорта белков плазмы крови в межклеточное пространство. Обычно это обусловлено повышением проницаемости стенок микрососудов при:
— развитии воспаления или местных аллергических реакций (под влиянием медиаторов воспаления и аллергии, например кининов, гистамина, серотонина);
— действии некоторых химических веществ (например, хлора, фосгена, люизита);
— попадании в ткань ядов насекомых и пресмыкающихся;
— воздействии ядов микробов (например, возбудителей дифтерии или сибирской язвы).
— Выхода в межклеточную жидкость белков клеток при их повреждении или разрушении (например, в очаге воспаления, при ишемии, аллергической реакции).
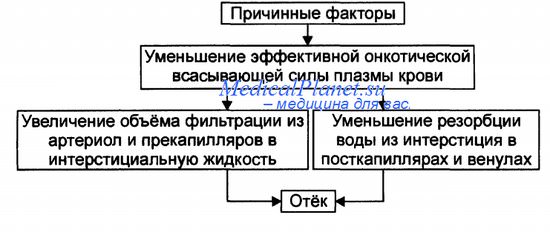
Механизм реализации онкотического фактора развития отёка.
— Увеличения гидрофильности белковых мицелл интерстициальной жидкости. Это может быть при:
— накоплении в интерстиции избытка некоторых ионов (например, Н+, К+, Na+);
— дефиците в межклеточном пространстве ионов Са2+;
— избытке БАВ (например, гистамина и серотонина);
— дефицита йодсодержащих тиреоидных гормонов.
Механизм реализации онкотического фактора заключается в уменьшении эффективной онкотической всасывающей силы (как следствие ги-попротеинемии и/или гиперонкии ткани). В результате возрастает объём фильтрации воды из микрососудов в интерстициальную жидкость по градиенту онкотического давления и уменьшается резорбция жидкости из межклеточного пространства в посткапиллярах и венулах.
— Читать далее «Осмотический фактор развития отека.»
Оглавление темы «Отеки. Причины и механизмы развития отеков.»:
1. Механизмы и принципы устранения гипергидратации.
2. Отёк. Виды отечной жидкости. Классификация отеков.
3. Факторы развития отеков. Гидродинамический фактор развития отеков.
4. Лимфогенный фактор развития отека.
5. Онкотический фактор развития отека.
6. Осмотический фактор развития отека.
7. Мембраногенный фактор развития отека.
8. Отеки при сердечной недостаточности.
9. Отек легких. Механизм развития отека легких.
10. Почечные отеки. Отёк при нефрозах.
Источник
Отёк — типовая форма нарушения водного обмена, характеризующаяся накоплением избытка жидкости вне сосудов: в межклеточном пространстве и/или полостях тела.
ВИДЫ ОТЁКОВ
Отёки дифференцируют в зависимости от их генеза, локализации, распространённости, скорости развития и по основному патогенетическому фактору развития отёка.
В зависимости от происхождения выделяют воспалительный и невоспалительный отёки.
• Воспалительный отёк образуется в результате экссудации под влиянием медиаторов воспаления (см. главу 5 «Воспаление»).
• Невоспалительный отёк связан с образованием транссудата.
Транссудат — бедная белком (менее 2%) и клеточными элементами отёчная жидкость.
В зависимости от локализации отёка различают анасарку и водянки.
• Анасарка — отёк подкожной клетчатки.
• Водянка — скопление транссудата в полости тела.
♦ Асцит — скопление транссудата в брюшной полости.
♦ Гидроторакс — накопление транссудата в плевральной полости.
♦ Гидроперикард — образование транссудата в полости околосердечной сумки.
♦ Гидроцеле — накопление транссудата между листками серозной оболочки яичка.
♦ Гидроцефалия — избыток жидкости в желудочках мозга (внутренняя водянка мозга) или в субарахноидальном пространстве (внешняя водянка мозга).
В зависимости от распространённости различают местный и общий отёки. В зависимости от скорости развитияотёка говорят о молниеносном или остром развитии, либо о хроническом течении отёка.
• Молниеносный отёк развивается в течение нескольких секунд после воздействия (например, после укуса насекомых или змей).
• Острый отёк развивается обычно в пределах часа после действия причинного фактора (например, отёк лёгких при острой сердечной недостаточности).
• Хронический отёк формируется в течение нескольких суток или недель (например, нефротический, отёк при голодании).
В зависимости от основного патогенетического фактора различают гидродинамический, лимфогенный, онкотический, осмотический и мембраногенный отёки.
Патогенетические факторы развития отёка ГИДРОДИНАМИЧЕСКИЙ ФАКТОР
Гидродинамический (гемодинамический, гидростатический) фактор характеризуется увеличением эффективного гидростатического давления в сосудах микроциркуляторного русла. Причины гемодинамического отёка.
• Повышение венозного давления.
♦ Системное венозное давление повышается при недостаточности сердца в связи со снижением его насосной функции.
♦ Местное венозное давление повышается при обтурации вен (например, тромбом или эмболом) или при их сдавлении (например, опухолью, рубцом, отёчной тканью).
• Увеличение ОЦК (например, вследствие гипоксии и увеличения выработки АДГ при хронической сердечной недостаточности).
Механизмы реализации гидродинамического фактора.
• Торможение резорбции интерстициальной жидкости в посткапиллярах и венулах в результате повышения эффективного гидростатического давления — разницы между гидростатическим давлением межклеточной жидкости (в среднем 7 мм. рт.ст.) и гидростатическим давлением крови в сосудах микроциркуляторного русла. В норме эффективное гидростатическое давление составляет в артериальной части микрососудов 36-38 мм рт.ст., а в венозной — 14-16 мм рт.ст.
Этот механизм играет главную роль при повышении венозного давления.
• Увеличение фильтрации крови в капиллярах вследствие повышения эффективного гидростатического давления. Как правило, этот механизм активируется при значительном возрастании ОЦК.
ЛИМФОГЕННЫЙ ФАКТОР
Лимфогенный (лимфатический) фактор характеризуется затруднением оттока лимфы от тканей вследствие либо механического препятствия, либо избыточного образования лимфы. Причины включения лимфогенного фактора.
♦ Врождённая гипоплазия лимфатических сосудов и узлов.
♦ Сдавление лимфатических сосудов (например, опухолью, рубцом, увеличенным соседним органом).
♦ Эмболия лимфатических сосудов (например, клетками опухоли, паразитами).
♦ Опухоль лимфоузла, а также метастазы в лимфоузел опухолей других органов.
♦ Повышение центрального венозного давления (например, при сердечной недостаточности или увеличении внутригрудного давления).
♦ Спазм стенок лимфатических сосудов (например, при выбросе избытка катехоламинов при феохромоцитоме, при стрессе).
♦ Значительная гипопротеинемия (содержание белков в плазме крови менее 35-40 г/л) и включение онкотического фактора формирования отёка. Вследствие возрастания тока жидкости из сосудов в интерстициальное пространство значительно повышается образование лимфы в тканях.
Механизмы развития лимфогенного отёка различны при динамической и механической лимфатической недостаточности.
• Динамическая лимфатическая недостаточность является результатом значительного возрастания лимфообразования. При этом лимфатические сосуды не способны транспортировать в общий кровоток существенно увеличенный объём лимфы. Наблюдается, например, при нефротическом синдроме, печёночной недостаточности.
• Механическая лимфатическая недостаточность является следствием механического препятствия оттоку лимфы по сосудам в результате их сдавления или обтурации, а также при увеличении центрального венозного давления. Формирование отёка конечностей по такому механизму обозначают как слоновость.
Гидродинамический и лимфогенный факторы развития отёка нередко объединяют единым термином — «механический» (поскольку причиной развития большинства их вариантов является механическое препятствие току крови или лимфы).
ОНКОТИЧЕСКИЙ ФАКТОР
Онкотический (гипоальбуминемический, гипопротеинемический) фактор развития отёка включается при снижении онкотического давления крови и увеличении его в межклеточной жидкости. Причины развития онкотического отёка.
♦ Снижение онкотического давления крови в результате гипопротеинемии (в основном за счёт гипоальбуминемии; альбумины примерно в 2,5 раза более гидрофильны, чем глобулины). Наиболее часто содержание альбуминов уменьшается при недостаточном поступлении или избыточной потере белков, снижении синтеза альбуминов в печени.
♦ Повышение онкотического давления интерстициальной жидкости при деструкции клеток и гидролизе протеинов межклеточной жидкости.
Механизм реализации онкотического фактора заключается в увеличении фильтрации жидкой части крови в капиллярах и уменьшении реабсорбции воды в посткапиллярах и венулах (как следствие гипопротеинемии и гиперонкии ткани).
ОСМОТИЧЕСКИЙ ФАКТОР
Осмотический фактор развития отёка запускается при повышении осмоляльности интерстициальной жидкости и снижении осмоляльности плазмы крови.
Причины развития осмотического отёка.
• Факторы, снижающие осмотическое давление крови и вызывающие развитие гипоосмолярной гипергидратации (см. выше).
• Факторы, повышающие осмоляльность интерстициальной жидкости:
♦ выход из повреждённых и разрушенных клеток осмотически активных веществ (ионов Na+, K+, Ca2+, глюкозы, МК, азотистых соединений);
♦ повышение диссоциации в интерстициальной жидкости солей и органических соединений (например, в условиях гипоксии или ацидоза);
♦ снижение транспорта осмотически активных веществ (ионов, органических и неорганических соединений) от тканей в результате замедления оттока крови по венулам;
♦ транспорт Na+ из плазмы крови в интерстициальную жидкость (например, при гиперальдостеронизме).
Механизм образования осмотического отёка заключается в избыточном транспорте воды из крови в межклеточную жидкость по градиенту осмотического давления. Данный механизм имеет место при сердечном, почечном (нефритическом), печёночном и ряде других отёков.
МЕМБРАНОГЕННЫЙ ФАКТОР
Мембраногенный фактор характеризуется существенным повышением проницаемости стенок сосудов микроциркуляторного русла для воды, мелко- и крупномолекулярных веществ.
Причины повышения проницаемости сосудистых стенок: ацидоз, активация гидролитических ферментов, перерастяжение стенок сосуда, изменение формы клеток эндотелия. Механизмы реализации мембраногенного фактора:
♦ облегчение фильтрации воды из крови в интерстициальное пространство. Этот механизм может быть сбалансирован повышением реабсорбции воды в посткапиллярах в связи с истончением их стенок;
♦ увеличение выхода молекул белка из плазмы крови в межклеточную жидкость ведёт к включению онкотического фактора. Такой механизм лежит в основе развития отёка при воспалении, местных аллергических реакциях, укусах насекомых и змей.
МНОГОФАКТОРНОСТЬ
В клинической практике, как правило, не встречаются монопатогенетические отёки (развивающиеся на основе только одного из описанных выше патогенетических факторов). В каждом конкретном случае в патогенезе отёка выделяют: 1) инициальный (стартовый, первичный) патогенетический фактор и 2) вторичные патогенетические факторы, включающиеся по ходу развития отёка, особенно при его хроническом течении.
Клинические варианты отёков ОТЁКИ ПРИ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ
Причина: сердечная недостаточность (состояние, при котором сердце не может адекватно обеспечить потребности органов и тканей в кровоснабжении).
Патогенез
Инициальный патогенетический фактор — гидродинамический.
• Последовательность включения и значимость других, указанных ниже, патогенетических факторов отёка могут быть различными в зависимости от динамики расстройств кровообращения и их последствий. К числу основных относятся: Уменьшение кровотока в сосудах почек.
♦ Причина: снижение величины минутного объёма кровотока.
♦ Механизм реализации: активация системы «ренин-ангиотензинальдостерон», вследствие чего усиливается реабсорбция Na+ в канальцах почек.
• Увеличение синтеза АДГ (гидродинамический фактор патогенеза отёка).
♦ Причина: увеличение реабсорбции Na+ в почках.
♦ Механизм реализации: гиперосмия крови (за счёт увеличения концентрации Na+) приводит к активации осморецепторов, усилению синтеза и высвобождения в кровь АДГ. Под влиянием этого гормона в почках увеличивается реабсорбция воды, что приводит к гиперволемии и включению гидродинамического фактора.
• Развитие механической лимфатической недостаточности (лимфогенный фактор).
♦ Причина: увеличение центрального венозного давления вследствие ослабления насосной функции сердца.
♦ Механизм реализации: торможение оттока лимфы из лимфатических протоков в венозную систему приводит к развитию механической лимфатической недостаточности (лимфогенный фактор).
• Увеличение осмотического давления в тканях (осмотический фактор патогенеза).
♦ Причины: венозный застой и лимфатическая недостаточность, изменение метаболизма в условиях гипоксии.
♦ Механизм реализации: увеличение образования метаболитов и снижение транспорта осмотически активных веществ от тканей приводит к повышению осмотического давления в интерстициальной жидкости и включению осмотического фактора.
• Повышение проницаемости сосудистой стенки (мембраногенный фактор).
♦ Причина: перерастяжение сосудов в условиях гиперволемии.
♦ Механизм реализации: облегчение фильтрации воды и повышение выхода белка из крови в интерстициальное пространство.
• Развитие печёночной недостаточности (онкотический фактор патогенеза).
♦ Причина: нарушение кровоснабжения печени.
♦ Механизмы реализации: расстройства энергетического, субстратного и кислородного обеспечения синтеза белка в гепатоцитах приводит к развитию гипоальбуминемии и включению онкотического фактора.
Таким образом, развитие отёка при сердечной недостаточности является результатом сочетанного и взаимопотенцирующего действия всех патогенетических факторов: гидродинамического, осмотического, онкотического, мембраногенного и лимфогенного.
ОТЁК ЛЁГКИХ
Как правило, отёк лёгких развивается весьма быстро. В связи с этим он чреват острой общей гипоксией и существенными расстройствами КЩР.
Причины
• Острая сердечная недостаточность (левожелудочковая или общая).
• Токсичные вещества, повышающие проницаемость стенок сосудов лёгких (например, фосген, фосфорорганические соединения, угарный газ, чистый кислород под высоким давлением).
Механизм развития
• Механизм развития отёка лёгких при сердечной недостаточности.
♦ Инициальный и основной патогенетический фактор — гемодинамический. При снижении сократительной функции миокарда левого желудочка кровь застаивается в сосудах малого круга кровообращения. При увеличении давления выше 25-30 мм рт.ст. вода начинает поступать в межклеточное пространство лёгких (развивается интерстициальный отёк).
♦ При накоплении в интерстиции большого количества отёчной жидкости она проникает между клетками эпителия альвеол, заполняя полости последних (развивается альвеолярный отёк). В связи с этим нарушается газообмен в лёгких, развиваются дыхательная гипоксия и ацидоз.
• Отёк лёгких при действии токсичных веществ. Инициальный и основной патогенетический фактор — мембраногенный. Под воздействием чистого кислорода или токсичных веществ увеличивается проницаемость стенок сосудов и изменяется форма эндотелия капилляров малого круга кровообращения.
ПОЧЕЧНЫЕ ОТЁКИ
Заболевания почек часто сопровождаются развитием отёчного синдрома. Патогенетические звенья образования отёков различны при нефритическом и нефротическом синдромах.
Отёк при нефротическом синдроме
Нефротический синдром развивается при патологии почек, как правило, первично невоспалительного генеза.
Инициальный патогенетический фактор отёка — онкотический.
• Причина отёка — потеря белка с мочой. Протеинурия (при нефротическом синдроме она может достигать 35-55 г в сутки) является следствием:
♦ Повышения проницаемости мембран почечных клубочков для белка, что сопровождается потерей не только альбуминов, но и глобулинов (трансферрина, гаптоглобина, церулоплазмина).
♦ Нарушения реабсорбции белков в канальцах почек.
• Звенья патогенеза:
♦ Снижение концентрации белка в плазме крови (гипопротеинемия) до 20-25 г/л (при норме 65-85 г/л).
♦ Увеличение фильтрации воды в капиллярах и накопление её избытка в межклеточном пространстве и полостях тела (онкотический фактор).
♦ Уменьшение эффективной онкотической всасывающей силы в посткапиллярах и венулах.
♦ Сдавление лимфатических сосудов отёчной тканью с развитием механической лимфатической недостаточности (лимфогенный фактор).
♦ Уменьшение ОЦК (гиповолемия).
♦ Снижение кровотока в почках (вызванное гиповолемией), активирует систему «ренин-ангиотензин-альдостерон». Это потенцирует реабсорбцию Na+ в почках.
♦ Увеличение [Na+] в плазме крови (гипернатриемия), приводящее к активации осморецепторов, усилению синтеза и высвобождения в кровь АДГ.
♦ Активация реабсорбции воды в канальцах почек.
♦ Увеличение эффективного гидростатического давления вследствие сдавления отёчной тканью венул, включающее гидростатический фактор.
Таким образом, в развитии нефротического отёка принимают участие преимущественно онкотический, гидростатический и лимфогенный факторы.
Отёк при нефритическом синдроме
Нефритический синдром развивается при заболеваниях почек первично воспалительного генеза.
Инициальный и основной патогенетический фактор — гидростатический.
• Причина отёка: нарушение кровоснабжения почек вследствие сдавления почечных сосудов экссудатом при воспалительных заболеваниях (например, при гломерулонефрите).
• Звенья патогенеза:
♦ Снижение кровотока в капиллярах клубочков приводит к уменьшению клубочковой фильтрации. Вследствие этого из плазмы крови выводится меньшее количество воды, чем в норме. Это вызывает увеличение ОЦК и включение гидродинамического фактора.
♦ Ишемия клеток юкстагломерулярного аппарата, приводящая к усилению синтеза и выделения в кровь ренина.
♦ Образование в крови под влиянием ренина ангиотензина I, который при участии ангиотензин-превращающего фермента (АПФ)
трансформируется в ангиотензин II. Этот процесс происходит в стенках сосудов (преимущественно в лёгких).
♦ Стимуляция ангиотензином II выделения клетками клубочковой зоны коры надпочечников альдостерона.
♦ Увеличение реабсорбции Na+ в канальцах почки с развитием гипернатриемии.
♦ Активация осморефлекса, сопровождающаяся выделением в кровь АДГ.
♦ Возрастание реабсорбции воды в канальцах почек с развитием гиперволемии, что способствует реализации гидростатического фактора.
В патогенезе нефритического отёка, помимо указанных выше, также могут принимать участие онкотический (при появлении протеинурии) и мембраногенный (при гломерулонефрите часто развивается генерализованный капилляриит) факторы.
Патогенная и адаптивная роль отёков
Патогенная роль отёков
• Механическое сдавление тканей.
♦ Обусловливает нарушение крово- и лимфооттока в результате сдавления сосудов.
♦ Вызывает болевые ощущения в связи с растяжением и смещением участков тканей и расположенных в них нервных окончаний.
• Нарушение обмена веществ между кровью и клетками с развитием различных дистрофий.
• Избыточный рост клеточных и неклеточных элементов соединительной ткани в зоне отёка с развитием склероза.
• Частое развитие инфекций в отёчной ткани. Механизм: подавление активности иммунных механизмов и факторов неспецифической защиты системы ИБН в условиях гипоксии и нарушения метаболизма.
• Нервно-психические расстройства (при отёке мозга).
• Расстройства КЩР вследствие образования избытка кислых продуктов анаэробного глик?
