Отек легких при дкмп

Дилатационная кардиомиопатия (ДКМП) – это тяжелое кардиологическое заболевание, приводящее к инвалидности в результате выраженного расширения камер сердца, что приводит к нарушению перекачивания крови. При этой болезни довольно быстро развивается сердечная недостаточность, и ей часто сопутствуют такие осложнения, как аритмия и тромбоэмболия.
Эпидемиология и встречаемость болезни
Из всех известных кардиомиопатий ДКМП является самой распространенной из них. Она встречается с частотой примерно 8 раз на 100 тыс. человек. В основном ею страдают люди в возрасте 30 – 40 лет, но есть и случаи среди маленьких детей и пожилых. Преимущественно болеют мужчины (отношение к женщинам составляет 3 – 4:1). Также недавние статистические исследования показали, что у населения негроидной расы ДКМП встречается в 2 раза чаще, чем у представителей европеоидной.
Почему возникает патология, и что происходит с сердцем
ДКМП занимает промежуточную позицию: она является чем-то средним между наследственным и приобретенным заболеванием. Примерно четверть (20 – 30%) всех случаев возникает из-за мутации генов, ответственных за образование белков мышечного цитоскелета кардиомиоцитов (дистрофин, ламинин). Они скрепляют все клетки миокарда в единое целое, обеспечивают передачу нервного импульса, а также синхронное сокращение всей сердечной мышцы.
При недостаточном образовании этих белков развивается постепенная дистрофия миокарда – ухудшается передача возбуждения от одной клетки к другой, и происходит медленное «ослабление» сердца как насосного органа. Генетическую природу дилатационной кардиомиопатии подтверждают многочисленные случаи среди близких родственников.
Наследственную ДКМП еще называют первичной или идиопатической. Приобретенные формы именуют вторичными. Причин данной разновидности заболевания довольно много, но за лидирующую позицию конкурируют две: миокардиты и алкоголизм.
Миокардиты
Примечательно то, что большую этиологическую роль играют именно вирусы. Все дело в том, что некоторые из них, особенно энтеровирусы (Коксаки А и В), помимо непосредственного повреждения кардиомиоцитов, способны запускать иммунопатологические процессы. Вследствие этого в организме начинают вырабатываться антимиокардиальные антитела, которые атакуют мышечные клетки сердца. Многие люди переносят вирусный миокардит и даже не подозревают об этом – его характерными признаками являются появление ноющих или колющих болей в области сердца, учащение сердцебиения через неделю после простудного заболевания.
В странах Южной и Центральной Америки самой частой причиной миокардита является болезнь Шагаса, вызываемая паразитом трипаносомой.
Алкоголизм
С алкоголем не все так однозначно, как может показаться на первый взгляд. Например, до 1960-х годов ДКМП была очень распространена среди людей, длительно употребляющих алкоголь. Причем в подавляющем большинстве случаев это были «любители» пива. И, разумеется, сначала именно спиртному приписывали роль причины развития ДКМП. После проведения исследований оказалось, что возникновение патологии связано с отравлением тяжелыми металлами, а именно кобальтом, который добавляли в пиво в качестве стабилизатора пены. В настоящее время кобальт в производстве напитка давно уже не используется.
И тем не менее, не стоит полностью отрицать токсическое действие больших доз алкоголя на сердце. До сих пор не до конца ясно, вызвано ли развитие ДКМП прямым повреждающим эффектом спиртного (а точнее, его токсичного метаболита – ацетальдегида) на сердечную мышцу, либо же причиной является недостаточное усвоение витамина В1 (тиамина) в желудочно-кишечном тракте у лиц, длительно употребляющих алкоголь.
Более редкие причины дилатационной кардиомиопатии следующие:
- эндокринологические заболевания – тиреотоксикоз, гипотиреоз, синдром/болезнь Иценко-Кушинга;
- использование лекарственных средств – наиболее сильным кардиотоксическим эффектом обладают противоопухолевые препараты Доксорубицин, Даунорубицин;
- дефицит питательных веществ – селена, карнитина, витамина Д;
- поражение сердца при системных заболеваниях – красная волчанка, анкилозирующий спондилоартрит (болезнь Бехтерева), амилоидоз, васкулиты и т. д.
Механизм развития болезни
В результате влияния различных этиологических факторов, будь то генетическая мутация или вирусный миокардит, камеры сердца начинают расширяться. Мышечные клетки постепенно гибнут, замещаясь соединительной тканью, развивается фиброз. Сердце становится менее эластичным, хуже растягивается в фазу диастолы, из-за чего желудочки плохо заполняются кровью. Оставшаяся ткань миокарда компенсаторно гипертрофируется, что в конечном счете приводит к его дистрофии и развитию сердечной недостаточности. В расширенных полостях сердца пациента с ДКМП образуются пристеночные тромбы.

Дилатационная кардиомиопатия у детей
ДКМП у детей занимает первое место среди всех кардиомиопатий. Она встречается примерно в 10 раз реже, чем у взрослых (частота – 0,5 на 100 000 людей), чаще болеют мальчики. Однако преобладающее число детских случаев патологии развивается вследствие генетических мутаций и протекает намного тяжелее, характеризуясь большей частотой летальных исходов.
Основные признаки
Клинические симптомы дилатационной кардиомиопатии складываются из признаков хронической (застойной) сердечной недостаточности (ХСН) и нарушений ритма сердца:
- Одышка – это самый первый и частый симптом ДКМП, который связан с застоем крови в сосудах легких. В самом начале заболевания она возникает только на фоне тяжкой физической работы, а при прогрессировании ДКМП появляется при обычной ходьбе и даже в покое. Одышка усиливается в ночное время, что связано с горизонтальным положением тела и застоем крови в легких. Иногда больные просыпаются среди ночи от удушья, поэтому они чувствуют себя немного лучше в сидячем или стоячем положении.
- Аритмии. Учащенное сердцебиение также является практически постоянным симптомом дилатационной кардиомиопатии. Она может возникать приступами либо протекать непрерывно. Иногда эпизод сопровождается довольно резким снижением артериального давления, из-за чего у больного начинает кружиться голова, появляется тошнота, ощущение «дурноты», он может даже упасть в обморок. Внеочередные сокращения сердца (экстрасистолы) пациентом воспринимаются как чувство «перебоев», «перекатывания органа в груди».
- Общая слабость. Мои пациенты с ДКМП часто жалуются на постоянное чувство усталости. У них быстро наступает утомляемость после, казалось бы, привычной физической работы.
- Тяжесть или боли в правом подреберье. Нередко из-за увеличения печени и застойных явлений в ней больные испытывают ноющий дискомфорт в правом боку под ребром.
- Отеки ног, особенно лодыжек, в вечернее время, из-за чего обувь становится тесной.
- Боли в области сердца. Характерны ноющие или сжимающие ощущения разной продолжительности (от нескольких секунд до часа). Могут возникать при физической нагрузке или в абсолютно спокойном состоянии.
Наиболее опасными осложнениями ДКМП являются тромбоэмболии, приводящие к инсульту, закупорке легочной артерии (ТЭЛА) и инфаркту других органов. Также нередко развивается внезапная смерть от дилатационной кардиомиопатии. Ее причиной выступают жизнеугрожающие нарушения ритма сердца: желудочковая тахикардия, фибрилляция желудочков, полная атриовентрикулярная блокада.
Как устанавливают диагноз: исследования и их критерии
Чтобы заподозрить наличие у человека дилатационной кардиомиопатии, я внимательно провожу его общий осмотр. Методом перкуссии я определяю границы сердца – прикладываю одну руку к грудной клетке больного и средним пальцем второй руки постукиваю по среднему пальцу первой, по звуку выявляя размеры органа. Из-за дилатации полостей сердца при ДКМП тупой звук имеет гораздо большую площадь, чем у здорового человека.
При аускультации сердца мне удается выслушать глухие тоны, высокую частоту сердечных сокращений (до 100 – 120 ударов в минуту), систолический шум на верхушке. На поздних стадиях болезни появляется дополнительный III тон между I и II, из-за чего возникает специфический «ритм галопа», свидетельствующий о тяжелом поражении сердечной мышцы.
После этого, чтобы провести дифференциальную диагностику с другими заболеваниями, я назначаю дополнительное обследование, включающее:
- электрокардиографию (ЭКГ);
- рентгенографию органов грудной клетки;
- эхокардиографию (ЭхоКГ, УЗИ сердца);
- определение в крови мозгового натрийуретического пептида (BNP, NT-proBNP).
На пленке ЭКГ я часто обнаруживаю различные нарушения ритма сердца: синусовую, суправентрикулярную или желудочковую тахикардию, фибрилляцию или трепетание предсердий, замедление предсердно-желудочковой проводимости (АВ-блокады), предсердные и желудочковые экстрасистолы. Так как многие аритмии протекают приступообразно (пароксзимально), иногда их не удается «поймать» при обычной записи, поэтому я дополнительно назначаю холтеровское (суточное мониторирование) ЭКГ.
На рентгене отчетливо можно увидеть расширенное сердце (кардиомегалию), усиление сосудистого рисунка из-за застоя крови в легочных сосудах.
Эхокардиография – это основной метод диагностики ДКМП. С его помощью можно определить точный размер увеличения каждой камеры сердца, а также измерить главный показатель сократительной (насосной) функции миокарда – фракцию левого желудочка.

При ДКМП практически всегда повышена концентрация мозгового натрийуретического пептида (BNP) и его предшественника (NT-proBNP). Первый выделяется в предсердиях, он участвует в регуляции объема циркулирующей крови. При задержке жидкости в сосудистом русле (что и происходит при сердечной недостаточности) предсердия растягиваются. В ответ на это начинает выделяться натрийуретический пептид, который усиливает выведение натрия с мочой, а вместе с ним уходит и лишняя жидкость из организма. Степень повышения этого гормона коррелирует с тяжестью сердечной недостаточности.
BNP и NT pro BNP повышается не только при ДКМП, но и при ХСН любого происхождения. Инструментально подтвержденные кардиомегалия и фракция выброса левого желудочка ниже 45 % – основные диагностические критерии ДКМП.
Методы лечения
Лечение дилатационной кардиомиопатии – это многоэтапный процесс. Первые пункты в нем – это ограничение физической нагрузки, уменьшение потребления поваренной соли до 3 грамм в сутки и полное исключение алкоголя. Без выполнения этих условий дальнейшая терапия окажется практически бесполезной. К сожалению, не существует медикаментозных способов лечения, позволяющих полностью избавиться от этого заболевания.
Хирургические вмешательства, применяющиеся при ДКМП:
- Сердечная ресинхронизирующая терапия. В правое предсердие и два желудочка устанавливаются электроды, подающие нервные импульсы, благодаря чему сердце начинает эффективнее сокращаться.
- Окутывание сердца мешком CorCap. Желудочки в буквальном смысле «окутываются» в эластичный сетчатый каркас, который препятствует патологическому расширению сердца, тем самым предотвращая прогрессирование ХСН. Этот метод в ряде случаев даже приводит к обратному развитию заболевания.
- Имплантация механических желудочков сердца. В полость левого желудочка устанавливается микронасос. Это позволяет добиться улучшения кровообращения всего организма.
- Трансплантация сердца – это наиболее радикальный метод лечения, позволяющий добиться полного исцеления от ДКМП. Данную операцию проводят пациентам до 60 лет при безуспешности других видов терапии.
Также для профилактики внезапной сердечной смерти в определенных условиях производится имплантация кардиовертера-дефибриллятора. Это специальное устройство, которое способно немедленно купировать возникающие жизнеугрожающие нарушения ритма сердца. Перспективным направлением в лечении ДКМП является пересадка стволовых клеток, благодаря чему происходит регенерация мышечных волокон. Данная методика находится еще на стадии клинических испытаний.
Поддержка пациента и устранение симптомов
Теперь разберем, какие же лекарства используются для борьбы с признаками ДКМП. Медикаментозная терапия имеет несколько направлений:
- замедление прогрессирования ХСН;
- лечение и профилактика нарушений ритма сердца;
- предотвращение тромбообразования.
Для лечения сердечной недостаточности я применяю следующие лекарственные препараты:
- Ингибиторы АПФ (Периндоприл, Лизиноприл) обязательно назначаются всем больным с ХСН. Эти лекарства улучшают сократительную функцию сердца, но при их приеме может возникнуть сухой кашель. В этом случае нужно провести замену на сартаны (Лозартан, Валсартан).
- Бета-адреноблокаторы (Бисопролол, Метопролол) тоже являются обязательными лекарствами. Они замедляют сердцебиение, благодаря чему сердечная мышца больше «отдыхает» и лучше кровоснабжается. Но стоит помнить, что они строго противопоказаны при полной АВ-блокаде (III степени), которая иногда развивается у пациентов с ДКМП.
- Калийсберегающие диуретики (Спиронолактон) – эти медикаменты выводят лишнюю жидкость из организма, что уменьшает дополнительную нагрузку на миокард.
- Мочегонные (Торасемид, Гидрохлортиазид) используются для выведения жидкости из организма.
Для лечения и профилактики нарушений ритма назначают антиаритмические средства (Амиодарон, Соталол). Если у больного имеется фибрилляция предсердий, я иногда использую сердечные гликозиды (Дигоксин).
Средняя продолжительность жизни
Дилатационная кардиомиопатия является тяжелым заболеванием. Продолжительность жизни пациентов с момента начала клинических признаков составляет от 2 до 10 лет в зависимости от степени прогрессирования. Основными причинами летального исхода являются хроническая сердечная недостаточность, тромбоэмболические осложнения и внезапная смерть от нарушений ритма сердца.
Источник
Кардиогенный отек легких – это патологическое состояние, которое характеризуется перфузией жидкости из легочных сосудов в интерстициальное пространство и альвеолы. Является следствием острой сердечной недостаточности. На начальном этапе болезни у пациента выявляется акроцианоз, тахикардия, одышка. По мере развития патологии из дыхательных путей начинает выделяться пена белого или розоватого цвета. Определяются признаки гипоксии. Диагноз выставляется на основании клинической картины и анамнестических данных. Лечение включает кислород, пропущенный через 70% этиловый спирт, ИВЛ, наркотические анальгетики, петлевые мочегонные, нитраты. По показаниям применяются кардиотоники, бронхолитики.
Общие сведения
Кардиогенный отек легких (КОЛ) – накопление жидкости в легочных пузырьках или интерстициальном пространстве. Обычно наблюдается у пациентов, имеющих кардиологический анамнез. Возникает в виде преходящего осложнения, купировать которое иногда удается на догоспитальном этапе. Вне зависимости от результатов оказания первой помощи пациент подлежит госпитализации в ОРИТ. Частота встречаемости у мужчин несколько выше, чем у женщин, соотношение – примерно 7:10. Это обусловлено несколько более поздним развитием атеросклероза и коронарной патологии у представительниц женского пола. Кардиогенный ОЛ может отмечаться при сердечной недостаточности любого происхождения, однако чаще диагностируется при ослаблении функции левого желудочка.
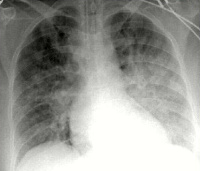
Кардиогенный отек легких
Причины
Нарушения в работе сердца возникают при органических изменениях органа, значительном увеличении ОЦК, под действием некардиогенных факторов. Определение первопричины – важный диагностический этап, поскольку от этиологии состояния зависит схема лечения. К числу заболеваний, при которых развивается отек сердечного происхождения, относятся:
- Левожелудочковая недостаточность (ЛН). Является истинным ухудшением сократительной способности сердца, чаще всего становится причиной гидротизации легких. Наблюдается при миокардитах, остром инфаркте миокарда, локализованном в соответствующей зоне, аортальном стенозе, коронарном склерозе, гипертонической болезни, недостаточности аортального клапана, аритмиях различного происхождения, ИБС.
- Увеличение ОЦК. Отмечается при острой почечной недостаточности, на фоне нарушения водного баланса. Жидкость, введенная больному внутривенно или употребленная им через рот, не выводится из организма, формируется КОЛ. Аналогичная ситуация создается при неверно подобранном объеме инфузионной терапии, тиреотоксикозе, анемии, циррозе печени.
- Легочная венозная обструкция. Причина – органические пороки развития венозной системы. Определяется при митральном стенозе, аномальном впадении легочных вен, их гипоплазии, формировании сосудистых мембран, фиброза. Кроме того, данное состояние возникает при наличии послеоперационных рубцов, сдавлении сосуда опухолью средостения.
- Некардиальные причины. Сердечные нарушения и, соответственно, пульмональный отек может стать результатом острого отравления кардиотоксическими ядами, нарушений мозгового кровообращения с поражением зон, отвечающих за работу сердца и сосудистый тонус, травм черепа. Патология нередко является симптомом шока любой этиологии.
Патогенез
Кардиогенный пульмональный отек имеет два механизма развития. При истинной левожелудочковой недостаточности происходит ослабление сократительной способности левого желудочка. Сердце оказывается не в состоянии перекачать всю кровь, поступающую из легочных вен. В последних возникает застой, повышается гидростатическое давление. Второй патогенетический механизм встречается при гипергидратации. Левый желудочек при этом работает нормально, однако его объем оказывается недостаточным для того, чтобы вместить в себя всю поступающую кровь. Дальнейшее развитие процесса не отличается от истинной разновидности ЛН.
Выделяют три этапа формирования КОЛ. На первом наблюдается растяжение крупных легочных сосудов, активное вовлечение в процесс венул и капилляров. Далее жидкость начинает скапливаться в интерстициальном пространстве. Раздражаются J-рецепторы интерстиция, появляется упорный кашель. В определенный момент соединительная ткань легких переполняется жидкостью, которая начинает пропотевать в альвеолы. Происходит вспенивание. Из 100 мл плазмы образуется до полутора литров пены, которая при кашле отделяется наружу через дыхательные пути.
Симптомы
Приступ чаще начинается ночью. Больной просыпается с ощущением удушья, принимает вынужденное полусидячее или сидячее положение с упором руками в кровать. Такая позиция способствует подключению вспомогательной мускулатуры и несколько облегчает дыхание. Возникает кашель, чувство нехватки воздуха, одышка более 25 вдохов в минуту. В легких выслушиваются различимые на расстоянии сухие свистящие хрипы, дыхание жесткое. Тахикардия достигает 100-150 уд/мин. При осмотре выявляется акроцианоз.
Переход интерстициального кардиогенного легочного отека в альвеолярный характеризуется резким ухудшением состояния пациента. Хрипы становятся влажными, крупнопузырчатыми, дыхание клокочущее. При кашле выделяется розоватая или белая пена. Кожа синюшная или мраморного оттенка, покрыта большим количеством холодного липкого пота. Отмечается беспокойство, психомоторное возбуждение, страх смерти, спутанность сознания, головокружение. Пульсовый разрыв между систолическим и диастолическим АД сокращается.
Уровень давления зависит от патогенетического варианта болезни. При истинной недостаточности левого желудочка систолическое АД снижается до показателей менее 90 мм рт. ст. Развивается компенсаторная тахикардия выше 120 ударов в минуту. Гиперволемический вариант протекает с подъемом артериального давления, увеличение ЧСС при этом сохраняется. Возникают сжимающие боли за грудиной, которые могут свидетельствовать о вторичном приступе ИБС, инфаркте миокарда.
Осложнения
Осложнения преимущественно связаны с гипоксией и гиперкапнией. При длительном течении болезни происходит ишемическое поражение клеток головного мозга (инсульт), что в дальнейшем приводит к интеллектуальным и когнитивным расстройствам, соматическим нарушениям. Недостаточное содержание кислорода в крови становится причиной кислородного голодания внутренних органов, что нередко заканчивается частичным или полным прекращением их деятельности. Наиболее опасна ишемия миокарда, которая может завершаться развитием инфаркта, фибрилляции желудочков, асистолии. На фоне кардиогенного отека иногда наблюдается присоединение вторичной инфекции и возникновение пневмонии.
Диагностика
Предварительный диагноз устанавливается бригадой скорой помощи. Дифференциация проводится с отеком легких несердечного происхождения. Определить причину болезни при первом контакте с пациентом затруднительно, поскольку клинические признаки КОЛ и патологии другого генеза практически не отличаются. Критерием постановки диагноза является наличие в анамнезе хронического сердечного заболевания, аритмии. В пользу несердечной причины свидетельствует наличие тиреотоксикоза, эклампсии, сепсиса, массивных ожогов, травм. В стационаре список диагностических мероприятий расширяется, пациенту показаны следующие обследования:
- Физикальное. При аускультации определяются сухие или влажные хрипы, при перкуссии отмечается появление «коробочного» звука. При сохраненном сознании больной занимает вынужденное положение, при психомоторном возбуждении мечется, не отдает себе отчета в происходящем.
- Лабораторное. В крови обнаруживаются признаки гипоксемии и гиперкапнии. SpО2 менее 90%, PaО2 менее 80 мм рт. ст., pH менее 7.35, лактат более 2 ммоль/литр. При гипергидратации уровень ЦВД превышает 12 мм водного столба. Если причиной патологии является инфаркт, в крови увеличиваются концентрации кардиоспецифического тропонина, КФК и КФК МВ.
- Инструментальное. На ЭКГ выявляются признаки пароксизмальных нарушений, острого коронарного синдрома, ишемии миокарда (коронарная т-волна, подъем сегмента ST). Рентгенография свидетельствует о снижении пневматизации полей легких по типу снежной бури, при альвеолярной разновидности просматривается затемнение в виде бабочки. На УЗИ сердца определяются признаки гипокинезии левого желудочка.
Лечение кардиогенного отека легких
Терапия на этапе медицинской эвакуации и в стационаре в целом не различается. Вне ЛПУ некоторые методы лечения могут быть проигнорированы из-за отсутствия технической возможности их реализации. Целью первой помощи является устранение клинических проявлений болезни, стабилизация состояния, транспортировка в кардиологическую реанимацию. В медицинском учреждении производят полную ликвидацию пневмонической гипергидратации и вызвавшей ее причины. К числу лечебных методик относятся:
- Оксигенотерапия. При транспортировке осуществляется введение пропущенного через 70% спирт кислорода посредством назальных канюль. В условиях стационара возможен перевод больного на искусственную вентиляцию легких со 100% O2. В качестве пеногасителя используется спирт или тифомсилан. Предпочтительным является инвазивный метод ИВЛ с интубацией трахеи. Вентиляция через маску не применяется в связи с высоким риском аспирации. Для повышения эффективности работы аппарата дыхательные пути очищают от пены с помощью электроотсоса.
- Дегидратация. Для разгрузки малого круга кровообращения и уменьшения ОЦК больной получает петлевые диуретики в высоких дозах. Назначается фуросемид и его аналоги. Использование маннита противопоказано, поскольку вначале он увеличивает поступление жидкости в сосудистое русло, что приводит к усугублению ситуации. По показаниям может быть проведена ультрафильтрация крови с отбором необходимого объема жидкой фракции.
- Анальгезия. Препарат выбора – морфин. Вводится внутривенно под контролем дыхания. Способствует устранению боли и тревожности, расширению сосудов большого круга, уменьшению нагрузки на легочные вены. При выраженном психомоторном возбуждении или болевом синдроме применяется нейролептанальгезия – сочетание наркотического анальгетика с антипсихотическим средством. При САД ниже 90 единиц наркотики и нейротропные препараты противопоказаны.
- Стимуляция сердца. Кардиотонические средства используются только при истинной ЛЖ. Препаратом выбора является дофамин, который подается титрованно через шприц-насос или инфузионную систему с дозатором. Для достижения инотропного эффекта требуются дозы менее 5 мг/кг/час. Для повышения АД дозировки должны превышать указанное значение. Вместо прессорных аминов могут назначаться сердечные гликозиды (коргликон, строфантин).
- Снижение ОПСС. Показаны нитраты (нитроглицерин). Медикаменты этой группы способствуют расширению периферических и коронарных артерий, облегчают работу сердца, способствуют уменьшению притока крови к легким. На этапе транспортировки применяются таблетированные сублингвальные формы, в стационаре выполняется внутривенное введение.
Лечение кардиогенного отека осуществляет врач-реаниматолог. При необходимости пациенту назначают консультации кардиолога или кардиохирурга, терапевта, пульмонолога. Во время пребывания больного в ОРИТ круглосуточно проводят мониторинг АД, ЧСС, ЧДД, SpO2, температуры тела. Ежедневно производят анализы биохимического состава крови, определяют КЩС и электролиты, маркеры острой коронарной патологии, при необходимости измеряют ЦВД.
Прогноз и профилактика
При своевременном начале лечения прогноз благоприятный, кардиогенный ОЛ удается купировать в 95% случаев. Отдаленные перспективы зависят от заболевания, ставшего причиной отека. При отсутствии медицинской помощи больной с высокой степенью вероятности погибает от острого нарушения кровообращения, шока, ишемии головного мозга и сердца. Специфические профилактические мероприятия отсутствуют. Следует своевременно осуществлять диагностику сосудистых и сердечных заболеваний, использовать все существующие возможности их лечения, соблюдать лечебно-охранительный режим, рекомендованный врачом.
Источник
