Наследственный ангионевротический отек рекомендации
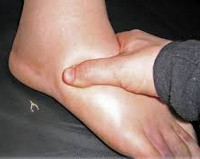
Наследственный ангионевротический отек – генетическое заболевание, при котором наблюдается дефицит ингибитора С1-компонента комплемента. Симптомами являются рецидивирующие отеки кожи, слизистых оболочек и органов брюшной полости, которые могут сопровождаться удушьем (при отеке гортани), рвотой и болями в животе (при поражении брюшной полости). Диагностика производится на основании осмотра, изучения наследственного анамнеза, определения С1-ингибитора, компонентов С4 и С2 в плазме крови, молекулярно-генетических исследований. Лечение осуществляется путем компенсирования абсолютного или функционального дефицита С1-ингибитора, применения блокаторов брадикинина и калликреина, использования свежезамороженной донорской плазмы.
Общие сведения
Наследственный ангионевротический отек (НАО) – вариант первичного иммунодефицита, обусловленный нарушением ингибирования системы комплемента, точнее, его основной фракции С1. Впервые это состояние было описано в 1888 году У. Осиером, который выявил рецидивирующие отеки у молодой женщины, а также установил, что подобное заболевание имелось как минимум у пяти поколений ее семьи. Примечательно, что собственно ангионевротический отек был открыт И. Квинке всего за 6 лет до обнаружения наследственной формы этой патологии – в 1882-м году. Наследственный ангионевротический отек имеет аутосомно-доминантный характер передачи и с одинаковой частотой поражает как мужчин, так и женщин. По некоторым данным, у женщин заболевание протекает тяжелее и возникает раньше, однако достоверных исследований по этому поводу не производилось. Встречаемость наследственного ангионевротического отека, по всей видимости, значительно варьирует у разных этнических групп, что дает весьма неоднородные цифры этого показателя – от 1:10 000 до 1:200 000.

Наследственный ангионевротический отек
Причины наследственного ангионевротического отека
Непосредственной причиной развития наследственного ангионевротического отека является первичный иммунодефицит, заключающийся в дефиците или функциональной неполноценности ингибитора эстеразы одного из компонентов комплемента – С1. В результате этого также нарушается ингибирование активации других компонентов этой системы – С4 и С2, что приводит к еще большему расстройству работы данного иммунного механизма. Врачам-генетикам удалось установить ген, отвечающий за 98% форм наследственного ангионевротического отека – им является C1NH, расположенный на 11-й хромосоме и кодирующий вышеуказанный ингибитор эстеразы С1. Различные мутации способны приводить к неодинаковым по своему течению формам заболевания, которые обладают достаточно сходными клиническими проявлениями, но различаются при проведении ряда диагностических тестов.
При одних типах мутации гена C1NH происходит полное прекращение синтеза белка-ингибитора С1, в результате чего он отсутствует в плазме крови, а остановка системы комплемента производится малоэффективными побочными путями. В других случаях наследственный ангионевротический отек возникает на фоне нормального содержания ингибитора в крови, при этом генетический дефект C1NH приводит к нарушению структуры активного центра данного фермента. В результате ингибитор С1 становится функционально неполноценным, что и служит причиной развития патологии. Существуют также редкие формы наследственного ангионевротического отека, при которых не наблюдается как изменений количества или активности ингибитора эстеразы С1, так и мутаций в гене C1NH – этиология и патогенез таких заболеваний на сегодняшний день неизвестны.
Остановка ингибирования активности компонентов комплемента (С1, С2, С4) приводит к запуску иммунной реакции, сходной по своему течению с аллергической, особенно крапивницей. Компоненты комплемента способны расширять кровеносные сосуды глубоких слоев дермы, повышать проницаемость их стенок, что провоцирует диффундирование компонентов плазмы крови в межклеточное пространство тканей кожи и слизистых оболочек и приводит к их отеку. Кроме того, немаловажную роль в патогенезе наследственного ангионевротического отека играют вазоактивные полипептиды – брадикинин и калликреин, которые еще больше увеличивают степень отека, а также способны вызывать спазм гладкомышечной мускулатуры органов желудочно-кишечного тракта. Эти процессы обуславливают все разнообразие симптомов наследственного ангионевротического отека: отечность кожи (в области конечностей, лица, шеи) и слизистых оболочек (ротовой полости, гортани, глотки), боли в животе и диспепсические расстройства, провоцируемые сочетанием отеков и спазмов.
Классификация наследственного ангионевротического отека
Всего на сегодняшний день выявлено три основных типа наследственного ангионевротического отека. Их различия в плане клинического течения патологии очень незначительны, для определения формы заболевания используют специальные диагностические методики. Врачу-иммунологу крайне важно выяснить тип наследственного ангионевротического отека, так как от этого во многом зависит тактика лечения данной патологии:
- Наследственный ангионевротический отек 1-го типа (НАО-1) – является наиболее распространенной формой заболевания, регистрируется у 80-85% больных с такой патологией. Причиной НАО этого типа является отсутствие гена C1NH или нонсенс-мутация в нем, в результате чего ингибитор С1 не образуется в организме.
- Наследственный ангионевротический отек 2-го типа (НАО-2) – более редкая форма патологии, выявляется лишь у 15% больных. Обусловлен также генетическим дефектом в C1NH, однако при этом экспрессия белка-ингибитора С1 не останавливается, а сам фермент имеет измененную структуру своего активного центра. Это приводит к его неполноценности, и он становится неспособен правильно выполнять свои функции.
- Наследственный ангионевротический отек 3-го типа – относительно недавно обнаруженная форма заболевания с практически неизученными этиологией и патогенезом. Достоверно удалось выяснить, что при этом типе отека отсутствуют мутации гена C1NH, сохраняется нормальное количество ингибитора эстеразы компонента комплемента С1 и его функциональная активность. Больше никаких данных по поводу данной формы (или их совокупности) наследственного ангионевротического отека не имеется.
Симптомы наследственного ангионевротического отека
Как правило, при рождении и в детском возрасте (за исключением редких случаев) наследственный ангионевротический отек ничем себя не проявляет. Довольно часто первые признаки заболевания возникают в подростковом периоде, так как их провоцируют стрессы и гормональные перестройки, происходящие в организме в это время. Однако нередко наследственный ангионевротический отек появляется позже – в возрасте 20-30 лет или даже у пожилых лиц. Чаще всего развитию первого приступа предшествует какое-либо провоцирующее явление: мощный эмоциональный стресс, серьезное заболевание, хирургическое вмешательство, прием некоторых лекарственных средств. В дальнейшем «порог чувствительности» по отношению к провоцирующим факторам снижается, приступы возникают все чаще – наследственный ангионевротический отек приобретает рецидивирующий характер.
Основным проявлением заболевания у большинства больных является отек кожи и подкожной клетчатки на кистях, стопах, иногда лице и шее. В более тяжелых случаях отечные явления возникают на слизистых оболочках полости рта, гортани и глотки – при этом может развиваться удушье (асфиксия), являющееся наиболее частой причиной смерти от наследственного ангионевротического отека. В других случаях на первый план выступают симптомы со стороны желудочно-кишечного тракта: тошнота, рвота, боли и рези в животе, иногда подобная клиническая картина приобретает черты «острого живота». В отдельных случаях наследственный ангионевротический отек характеризуется сочетанием отека кожи, слизистых оболочек и поражения желудочно-кишечного тракта.
Диагностика наследственного ангионевротического отека
Для выявления наследственного ангионевротического отека используют данные физикального осмотра больного, изучения его наследственного анамнеза, определения в крови количества ингибитора С1, а также компонентов комплемента С1, С2, С4, и молекулярно-генетических исследований. Осмотр в фазу обострения заболевания выявляет отек кожи или слизистых оболочек, пациенты могут жаловаться на боли в животе, рвоту, диарею. В крови при наличии наследственного ангионевротического отека 1-го типа ингибитор эстеразы С1 полностью отсутствует, значительно снижены концентрации индикаторных компонентов комплемента. При 2-м типе заболевания в плазме крове может определяться незначительное количество ингибитора С1, в редких случаях его уровень соответствует норме, но соединение имеет пониженную функциональную активность. При всех трех вариантах наследственного ангионевротического отека уровень С1, С2 и С4 не превышает 30-40% от нормы, поэтому этот показатель является ключевым в диагностике данного состояния.
Изучение наследственного анамнеза пациента зачастую обнаруживает наличие подобного заболевания как минимум у нескольких поколений его предков и у других родственников. Однако отсутствие признаков семейного характера патологии не является однозначным критерием, позволяющим исключить наследственный ангионевротический отек – примерно у четверти больных это состояние обусловлено спонтанными мутациями и выявляется впервые в семье. Молекулярно-генетическая диагностика осуществляется путем автоматического секвенирования гена C1NH с целью выявления мутаций. Дифференциальную диагностику следует производить с ангионевротическим отеком аллергического генеза и приобретенными формами дефицита ингибитора С1.
Лечение наследственного ангионевротического отека
Терапию наследственного ангионевротического отека разделяют на два типа – лечение для купирования острого приступа заболевания и профилактический прием препаратов для предупреждения их развития. В случае острого отека Квинке, обусловленного НАО, традиционные противоанафилактические меры (адреналин, стероиды) неэффективны, необходимо использовать нативный или рекомбинантный ингибитор С1, антагонисты брадикинина и калликреина, при их отсутствии показано переливание свежезамороженной плазмы. Начинать такое лечение нужно как можно раньше, в идеале – при самых первых приступах наследственного ангионевротического отека.
Долгосрочная профилактика заболевания производится в тех случаях, когда приступы возникают слишком часто (чаще раза в месяц), если в анамнезе имелись случаи отека гортани или удушья, либо госпитализация в реанимационное отделение. Профилактика включает в себя использование андрогенов, экзогенных (рекомбинантных или нативных) форм ингибитора эстеразы С1, антифибринолитических препаратов. При доброкачественном течении наследственного ангионевротического отека – редких приступах и их относительно быстром исчезновении – такое лечение может не назначаться. Однако накануне хирургических или стоматологических вмешательств, физических и умственных нагрузок рекомендуется краткосрочно принимать вышеуказанные средства для уменьшения риска развития приступа.
Прогноз и профилактика наследственного ангионевротического отека
В большинстве случаев прогноз наследственного ангионевротического отека относительно благоприятный в плане выживаемости – при разумном лечении и профилактике приступы возникают крайне редко и не угрожают жизни больного. При этом всегда сохраняется риск отека гортани, что может привести к асфиксии и летальному исходу. Таким больным следует не только избегать значительных физических и эмоциональных нагрузок, но и желательно иметь при себе карточку или медальон с указанием диагноза. Огромное количество смертей от наследственного ангионевротического отека было обусловлено неверными действиями медиков, не знающих диагноза и поэтому использующих традиционные при аллергическом отеке Квинке препараты, которые неэффективны при НАО.
Источник
Введение
Наследственный ангионевротический отек (НАО) — редкое, потенциально жизнеугрожающее, генетически детерминированное заболевание с аутосомно-доминантным типом наследования, встречающееся примерно у 1 из 50 000 человек [1–4]. Мутация в гене SERPING1 приводит к дефициту количества ингибитора С1-эстеразы и/или снижению его функциональной активности. При раннем дебюте НАО у многих пациентов он тем не менее остается нераспознанным на протяжении десятков лет. Типичными ошибочными диагнозами являются аллергический или идиопатический ангионевротический отек, а в некоторых случаях — анафилаксия.
Основными симптомами НАО выступают отеки кожи и слизистых/подслизистых оболочек, вызываемые брадикинином, который высвобождается под действием самых разнообразных триггеров [1]. Характерной особенностью НАО является отсутствие зуда, гиперемии кожи, сопутствующей крапивницы, а также клинического эффекта от лечения системными глюкокортикостероидами (ГКС) и антигистаминными препаратами (АГП) [1, 4].
Для профилактики развития отеков больным НАО назначаются андрогены (даназол) или антифибринолитические препараты [1, 5]. Для лечения приступов НАО применяют икатибант (Фиразир) — блокатор В2-рецепторов брадикинина. Для краткосрочной профилактики и лечения атак применяется также ингибитор С1-эстеразы человека [1, 6, 7].
По данным литературных источников, больные НАО крайне редко имеют сопутствующие аллергические заболевания. Однако бывают единичные случаи совместных проявлений НАО и атопии [8].
Приводим описание такого случая.
Клиническое наблюдение
Больная Г., 30 лет, была осмотрена врачом аллергологом-иммунологом частного медицинского центра после многочисленных консультаций врачей других специальностей.
Из анамнеза: до года росла и развивалась соответственно возрасту. Вакцинирована в детстве согласно календарю прививок без реакций и осложнений. С 7-летнего возраста стали беспокоить периодические приступы кашля при контакте с домашней пылью. Симптомы были достаточно легкими и проходили самостоятельно без приема АГП. С 10 лет присоединились симптомы атопического конъюнктивита. С 25 лет стали проявляться легкие симптомы сезонного аллергического риноконъюнктивита (апрель — май, июль — сентябрь).
Наследственный анамнез отягощен по сахарному диабету 2 типа (бабушка со стороны матери). У сестры в детстве периодически отмечалась отечность губы (проходила самостоятельно, к врачу не обращалась); с возрастом добавились симптомы холодовой крапивницы. У сына наблюдаются проявления аллергического риноконъюнктивита (на домашнюю пыль и пыльцу деревьев).
Из акушерско-гинекологического анамнеза: в 2008 г. у пациентки был выкидыш; в 2009 г. — оперативные роды (ребенок — живой мальчик). Повторное кесарево сечение в 2016 г. (ребенок — живая девочка), после чего спустя 3 мес. появились тянущие боли в низу живота с позывами на мочеиспускание. На осмотре врачом-гинекологом при болях в животе пальпаторно отмечалась выраженная болезненность (цитологическое исследование: норма; при ультразвуковом исследовании: отечность органов малого таза). Далее наблюдалась у гинеколога с диагнозом «аденомиоз» и с 2018 по 2019 г. получала оральные контрацептивы. Периодичность абдоминальных болей была 1 раз в 3–4 мес. В 2018 г. было несколько эпизодов «цистита», сопровождавшихся внезапной болью в области половых органов. В комплексную терапию пациентки всегда включались курсы антибактериальных препаратов; при этом, со слов женщины, врачи всякий раз сомневались в целесообразности таких назначений, т. к. результаты анализов всегда были в пределах нормы.
В октябре 2017 г. больной были установлены 4 зубных титановых имплантата и удален зуб, после чего у пациентки сразу же увеличились шейные и подчелюстные лимфатические узлы. Была осмотрена стоматологом и челюстно-лицевым хирургом, проведена антибактериальная терапия и местное лечение димексидом. Осмотрена гематологом, который не нашел данных за болезнь крови. В феврале 2018 г. после механического воздействия в области бедра возник отек, плотный на ощупь, зудящий, без изменения цвета кожи, сохранявшийся на протяжении 7–10 дней. Затем (с апреля 2018 г.) практически ежемесячно стали беспокоить отеки разной локализации (подмышечная область, спина, ноги), сопровождавшиеся периодически незначительным зудом. Отеки всегда были плотные на ощупь, с четкими границами, с небольшой гиперемией на 2-й день (когда отек начинал увеличиваться), болезненные, негорячие на ощупь и самостоятельно проходили за 3–4 дня. На фоне месячной терапии ГКС и АГП (без существенной динамики) отеки рецидивировали. Пациентка была осмотрена дерматологом, хирургом, неврологом, гематологом, сосудистым хирургом — диагноз не был установлен. В течение 2018 г. больная получила 15 курсов антибиотиков.
В ноябре 2018 г. на фоне «полного здоровья» появился выраженный отек правой кисти, сопровождавшийся зудом, нараставший в течение нескольких часов. Бригадой скорой медицинской помощи были введены ГКС и АГП, эффект отсутствовал. На следующие сутки отек распространился на предплечье и сохранялся в течение недели. В декабре 2018 г. во время имплантации зуба появилась отечность лица, в т. ч. губ, нараставшая в течение суток, затем прошла самостоятельно в течение недели.
В январе 2019 г. обратилась на консультацию к аллергологу-иммунологу, было проведено обследование и выявлены следующие отклонения: анемия легкой степени тяжести (гемоглобин 101 г/л), анизоцитоз (микро), незначительная гипохромия, эозинофилия (13,9%, абс. количество: 870 кл/мкл); С4-компонент комплемента 0,06 г/л (норма: 0,15–0,57 г/л); антитела к С1q комплемента 14,03 отн. ед/мл (норма: до 10 отн. ед/мл), ингибитор С1-эстеразы 0,52 Ед/мл (норма: 0,7–1,3 Ед/мл). Анализ крови на специфические IgE к аллергенам (RIDA, Санкт-Петербург, апрель 2019 г.) выявил сенсибилизацию к пыльце березы — 1,11 МЕ/мл, ольхи — 1,66 МЕ/мл, смеси трав — 2,12 МЕ/мл, ржи — 2,91 МЕ/мл, к моркови — 0,93 МЕ/мл, пшенице (мука) — 1,23 МЕ/мл, клещу домашней пыли (Dermatophagoides farinae) — 0,83 МЕ/мл (норма: до 0,34 МЕ/мл). Уровень общего IgE — менее 25 МЕ/мл (норма: до 100 МЕ/мл). Сенсибилизация к пыльце деревьев и клещам домашней пыли совпадала с данными аллергологического анамнеза.
При дообследовании в ФБУН НИИ эпидемиологии и микробиологии имени Пастера (центральная клинико-диагностическая лаборатория) методом иммунотурбидиметрии: ингибитор С1-эстеразы количественный 33,4 мг/дл (норма: 23–41 мг/дл), функциональная активность 9,38% (норма: 70–130%), С4 0,36 г/л (норма: 0,09–0,36 г/л). В ФГБНУ «МГНЦ» (лаборатория молекулярно-генетической диагностики) было проведено исследование ДНК на наличие мутаций в гене SERPING1 (C1NH) и обнаружены 2 неописанных варианта неопределенного клинического значения в гетерозиготном состоянии: с.874G>C (Ala292Pro) и c.889+81(IVS5+81G>C). Такие же мутации в вышеуказанном гене были выявлены у сестры, матери и сына пациентки (при дальнейшем исследовании в той же лаборатории). При проведении исследования ДНК на наличие протяженных делеций/дупликаций экзонов гена SERPING1 (C1NH) методом количественной MLPA экзонов (1–8) гена SERPING1 изменения числа копий последовательности не обнаружены.
В марте 2019 г. у пациентки развился острый пиелонефрит, сопровождавшийся отеком передней брюшной стенки.
В результате проведенного обследования был установлен основной диагноз: Первичный иммунодефицит: дефект в системе комплемента (D84.1). Наследственный ангиоотек 1 типа (мутация в гене SERPING1 с.874G>C (Ala292Pro), c.889+81(IVS5+81G>C)).
Сопутствующие заболевания: аллергический риноконъюнктивит легкого персистирующего течения; сенсибилизация к аллергенам пыльцы деревьев, злаковых трав, клещам домашней пыли; анемия легкой степени тяжести.
В мае 2019 г. пациентка была поставлена на диспансерный учет у аллерголога-иммунолога и терапевта по месту жительства. В соответствии с Федеральными клиническими рекомендациями по НАО (2019 г.) для купирования атак был рекомендован икатибант (шприц-ручка); для краткосрочной профилактики и купирования атак — концентрат ингибитора С1-эстеразы [1]. Заявка на препараты осуществлялась ежемесячно по мере потребности, в зависимости от частоты атак. За полгода было использовано 2 шприц-ручки икатибанта и 4 флакона ингибитора С1-эстеразы. Для базисной терапии был рекомендован даназол 200 мг 1 р./сут.
При назначении транексамовой кислоты в дозе 1 г/сут отмечались побочные реакции в виде головокружения, ухудшения самочувствия, выраженной болезненности в брюшной полости во время очередной атаки. В августе 2019 г. через 5 дней после установки зубных имплантатов (по решению пациентки без предварительной консультации аллерголога-иммунолога и без краткосрочной профилактики) появилась резкая боль в шее, голове, повысилось артериальное давление до 160/90 мм рт. ст., наблюдалась потеря сознания с судорогами Через 4 ч от начала атаки внутривенно был введен концентрат ингибитора С1-эстеразы (соответственно массе тела пациентки). Состояние стабилизировалось постепенно, в течение 3 сут сохранялась выраженная головная боль. В сентябре на фоне пиелонефрита с затрудненным мочеиспусканием вновь появился отек передней брюшной стенки. В результате внутривенного введения концентрата ингибитора С1-эстеразы ожидаемого эффекта не последовало. Через 33 дня (отмечена четкая связь с менструальным циклом) на фоне повышения температуры тела до фебрильных цифр и боли в горле на 2-й день
отмечены затрудненное глотание, уплотнение в области шеи. На фоне введения икатибанта болезненность в шее уменьшилась через 30 мин, отечность спала в течение суток. В ноябре 2019 г. была потеря сознания с судорогами; сразу был введен икатибант, и в течение одного часа состояние нормализовалось. В январе 2020 г. при обследовании в отделении иммунопатологии ФГБУ «ГНЦ Институт иммунологии» ФМБА России: С4 компонент комплемента 0,02 мг/мл (норма: 0,2–0,55 мг/мл), количественный уровень ингибитора С1-эстеразы составил 2,3 мг/дл (норма: 15–35 мг/дл), функциональная активность менее 5% (норма: 70–130%). В результате дообследования пациентке был установлен диагноз: НАО 1 типа.
Заключение
Данный клинический случай демонстрирует редкое сочетание дефекта в системе комплемента (дефицит ингибитора С1-эстеразы человека) и атопии (с детства у пациентки и ее сына отмечался аллергический риноконъюнктивит; увеличивалась концентрация в крови пациентки специфических IgE к пыльце растений и клещам домашней пыли; отмечена связь симптомов риноконъюнктивита с реакцией на домашнюю пыль и пыльцу растений). Кроме того, особенностью данного случая явились разнообразие локализаций ангиоотеков (голова, шея, глотка, мочеполовая система, конечности) и большое число курсов антибиотиков (15 за 2018 г.). Необходимо отметить, что пациентка осматривалась терапевтом, гинекологом, стоматологом, дерматологом, хирургом, неврологом, гематологом, сосудистым хирургом, но никто из специалистов не заподозрил НАО. В диагностике НАО большое значение имеют тщательный сбор анамнеза и анализ объективных данных, выявление семейной предрасположенности и оценка ответа на терапию системными ГКС и АГП.
В связи с указанными трудностями следует подчеркнуть актуальность просвещения врачей разных специальностей, особенно стоматологов, оториноларингологов, хирургов, гастроэнтерологов, гинекологов, анестезиологов-реаниматологов, терапевтов, педиатров относительно комплемент-зависимых ангиоотеков, НАО, что поможет существенно улучшить выявляемость таких состояний. От ранней диагностики НАО зависят своевременное назначение эффективных для комплемент-зависимых ангиоотеков лекарственных средств и отмена ненужных препаратов.
В настоящее время проведение своевременной и адекватной терапии НАО способно значительно улучшить качество жизни больных. Наличие таких препаратов, как икатибант (Фиразир), в бесплатном для пациентов доступе (при своевременной постановке таких больных на учет по программе орфанных заболеваний) позволяет избежать летальных исходов [9, 10].
Благодарность
Компания ООО «Такеда Фармасьютикалз» поддерживала техническую редакцию статьи и обеспечивала взаимодействие между авторами настоящей публикации.
Acknowledgement
Technical edition and cooperation between the authors is supported by LLC “Takeda Pharmaceuticals”.
Сведения об авторах:
1Андронова Елена Владимировна — врач аллерголог-иммунолог, ORCID iD 0000-0002-9506-6365;
2Бельтюков Евгений Кронидович — д.м.н., профессор кафедры факультетской терапии, эндокринологии, аллергологии и иммунологии, ORCID iD 0000-0003-2485-2243;
2,3Лепешкова Татьяна Сергеевна — к.м.н., ассистент кафедры поликлинической педиатрии и педиатрии ФПК и ПП, врач
аллерголог-иммунолог, ORCID iD 0000-0002-0716-3529.
1ООО «Семейный доктор». 455034, Россия, г. Магнитогорск, ул. Жукова, д. 11.
2ФГБОУ ВО УГМУ Минздрава России. 620028, Россия,
г. Екатеринбург, ул. Репина, д. 3.
3МАУ «ДГП № 13». 620100, Россия, г. Екатеринбург,
ул. Ткачей, д. 16а.
Контактная информация: Андронова Елена Владимировна, e-mail: andronova.elena_@mail.ru. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 21.02.2020.
About the authors:
1Elena V. Andronova — MD, allergist and immunologist,
ORCID iD 0000-0002-9506-6365;
2Evgeniy K. Bel’tyukov — MD, PhD, Professor of the Department of Faculty Therapy, Endocrinology, Allergy, and Immunology, ORCID iD 0000-0003-2485-2243;
2,3Tat’yana S. Lepeshkova — MD, PhD, Assistant of the Department of Polyclinic Pediatrics and Pediatrics, allergist and immunologist, ORCID iD 0000-0002-0716-3529.
1LLC “Family doctor”. 11, Zhukova str., Magnitogorsk, 455034, Russian Federation.
2Ural State Medical University. 3, Repin str., Yekaterinburg, 620028, Russian Federation.
3Children’s City Polyclinic No. 13. 16a, Tkachey str., Yekaterinburg, 620100, Russian Federation.
Contact information: Elena V. Andronova, e-mail:
andronova.elena_@mail.ru. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 21.02.2020.
Источник
