Мембраногенный фактор при отеке
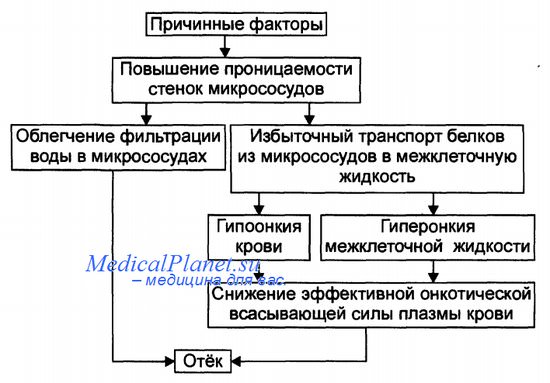
Мембраногенный фактор характеризуется существенным повышением проницаемости стенок сосудов микроциркуляторного русла для воды, мелко- и крупномолекулярных веществ (наибольшее значение среди последних имеют белки).
• Причины повышения проницаемости стенок микрососудов перечислены на рисунке.
— Ацидоз. В условиях значительного увеличения концентрации ионов Н+ возрастает неферментный («кислотный») гидролиз основного вещества базальной мембраны сосудистой стенки. Это и приводит к её разрыхлению и как следствие — к возрастанию проницаемости.
— Повышение активности гидролитических ферментов в стенке микрососудов и/или прилегающих к ним тканях. Это интенсифицирует процесс ферментативного гидролиза гликозаминогликанов, а также волокнистых структур сосудистой стенки. Такая картина наблюдается при выраженной гипоксии, ацидозе, при воздействии так называемых лабилизаторов лизосом (например, лизофосфолипидов, продуктов липопероксидации, протеоли-тических ферментов).

Механизм реализации мембраногенного фактора развития отёка.
— Перерастяжение стенок микрососудов. Это наблюдается при:
— Развитии артериальной гиперемии нейромиопаралитического типа (т.е. в условиях длительного снижения нейрогенного и мышечного тонуса артериол и прекапилляров).
— Венозной гиперемии и лимфостазе.
Механизмы реализации мембраногенного фактора развития отёка.
— Облегчение фильтрации воды. В связи с этим увеличивается выход жидкости из крови и лимфы в интерстициальное пространство. Однако этот механизм может быть сбалансирован повышением реабсорбции воды в венозном отделе капилляров в связи с истончением их стенок.
— Увеличение выхода молекул белка из микрососудов в межклеточную жидкость. Это ведёт к снижению онкотического давления плазмы крови и лимфы и одновременно к развитию гиперонкии межклеточной жидкости. В условиях повышенной проницаемости стенок микрососудов жидкость из них интенсивно поступает в межклеточное пространство по градиенту онкотического давления. Именно такой механизм (помимо других) лежит в основе развития отёка тканей при их воспалении, местных аллергических реакциях, укусах насекомых и змей, действии некоторых отравляющих веществ, чистого кислорода, особенно при избыточном атмосферном давлении.
Многофакторность
В клинической практике, как правило, не встречаются отёки, развивающиеся на основе только одного из описанных выше патогенетических факторов (иначе говоря, нет монопатогенетических отёков). В связи с этим в каждом конкретном случае при наличии отёка выделяют: 1) инициальный (стартовый, первичный) патогенетический фактор у данного пациента и 2) патогенетические факторы, включающиеся в процессе развития отёка вторично.
— Читать далее «Отеки при сердечной недостаточности.»
Оглавление темы «Отеки. Причины и механизмы развития отеков.»:
1. Механизмы и принципы устранения гипергидратации.
2. Отёк. Виды отечной жидкости. Классификация отеков.
3. Факторы развития отеков. Гидродинамический фактор развития отеков.
4. Лимфогенный фактор развития отека.
5. Онкотический фактор развития отека.
6. Осмотический фактор развития отека.
7. Мембраногенный фактор развития отека.
8. Отеки при сердечной недостаточности.
9. Отек легких. Механизм развития отека легких.
10. Почечные отеки. Отёк при нефрозах.
Источник
Отёк — типовая форма нарушения водного обмена, характеризующаяся накоплением избытка жидкости вне сосудов: в межклеточном пространстве и/или полостях тела.
ВИДЫ ОТЁКОВ
Отёки дифференцируют в зависимости от их генеза, локализации, распространённости, скорости развития и по основному патогенетическому фактору развития отёка.
В зависимости от происхождения выделяют воспалительный и невоспалительный отёки.
• Воспалительный отёк образуется в результате экссудации под влиянием медиаторов воспаления (см. главу 5 «Воспаление»).
• Невоспалительный отёк связан с образованием транссудата.
Транссудат — бедная белком (менее 2%) и клеточными элементами отёчная жидкость.
В зависимости от локализации отёка различают анасарку и водянки.
• Анасарка — отёк подкожной клетчатки.
• Водянка — скопление транссудата в полости тела.
♦ Асцит — скопление транссудата в брюшной полости.
♦ Гидроторакс — накопление транссудата в плевральной полости.
♦ Гидроперикард — образование транссудата в полости околосердечной сумки.
♦ Гидроцеле — накопление транссудата между листками серозной оболочки яичка.
♦ Гидроцефалия — избыток жидкости в желудочках мозга (внутренняя водянка мозга) или в субарахноидальном пространстве (внешняя водянка мозга).
В зависимости от распространённости различают местный и общий отёки. В зависимости от скорости развитияотёка говорят о молниеносном или остром развитии, либо о хроническом течении отёка.
• Молниеносный отёк развивается в течение нескольких секунд после воздействия (например, после укуса насекомых или змей).
• Острый отёк развивается обычно в пределах часа после действия причинного фактора (например, отёк лёгких при острой сердечной недостаточности).
• Хронический отёк формируется в течение нескольких суток или недель (например, нефротический, отёк при голодании).
В зависимости от основного патогенетического фактора различают гидродинамический, лимфогенный, онкотический, осмотический и мембраногенный отёки.
Патогенетические факторы развития отёка ГИДРОДИНАМИЧЕСКИЙ ФАКТОР
Гидродинамический (гемодинамический, гидростатический) фактор характеризуется увеличением эффективного гидростатического давления в сосудах микроциркуляторного русла. Причины гемодинамического отёка.
• Повышение венозного давления.
♦ Системное венозное давление повышается при недостаточности сердца в связи со снижением его насосной функции.
♦ Местное венозное давление повышается при обтурации вен (например, тромбом или эмболом) или при их сдавлении (например, опухолью, рубцом, отёчной тканью).
• Увеличение ОЦК (например, вследствие гипоксии и увеличения выработки АДГ при хронической сердечной недостаточности).
Механизмы реализации гидродинамического фактора.
• Торможение резорбции интерстициальной жидкости в посткапиллярах и венулах в результате повышения эффективного гидростатического давления — разницы между гидростатическим давлением межклеточной жидкости (в среднем 7 мм. рт.ст.) и гидростатическим давлением крови в сосудах микроциркуляторного русла. В норме эффективное гидростатическое давление составляет в артериальной части микрососудов 36-38 мм рт.ст., а в венозной — 14-16 мм рт.ст.
Этот механизм играет главную роль при повышении венозного давления.
• Увеличение фильтрации крови в капиллярах вследствие повышения эффективного гидростатического давления. Как правило, этот механизм активируется при значительном возрастании ОЦК.
ЛИМФОГЕННЫЙ ФАКТОР
Лимфогенный (лимфатический) фактор характеризуется затруднением оттока лимфы от тканей вследствие либо механического препятствия, либо избыточного образования лимфы. Причины включения лимфогенного фактора.
♦ Врождённая гипоплазия лимфатических сосудов и узлов.
♦ Сдавление лимфатических сосудов (например, опухолью, рубцом, увеличенным соседним органом).
♦ Эмболия лимфатических сосудов (например, клетками опухоли, паразитами).
♦ Опухоль лимфоузла, а также метастазы в лимфоузел опухолей других органов.
♦ Повышение центрального венозного давления (например, при сердечной недостаточности или увеличении внутригрудного давления).
♦ Спазм стенок лимфатических сосудов (например, при выбросе избытка катехоламинов при феохромоцитоме, при стрессе).
♦ Значительная гипопротеинемия (содержание белков в плазме крови менее 35-40 г/л) и включение онкотического фактора формирования отёка. Вследствие возрастания тока жидкости из сосудов в интерстициальное пространство значительно повышается образование лимфы в тканях.
Механизмы развития лимфогенного отёка различны при динамической и механической лимфатической недостаточности.
• Динамическая лимфатическая недостаточность является результатом значительного возрастания лимфообразования. При этом лимфатические сосуды не способны транспортировать в общий кровоток существенно увеличенный объём лимфы. Наблюдается, например, при нефротическом синдроме, печёночной недостаточности.
• Механическая лимфатическая недостаточность является следствием механического препятствия оттоку лимфы по сосудам в результате их сдавления или обтурации, а также при увеличении центрального венозного давления. Формирование отёка конечностей по такому механизму обозначают как слоновость.
Гидродинамический и лимфогенный факторы развития отёка нередко объединяют единым термином — «механический» (поскольку причиной развития большинства их вариантов является механическое препятствие току крови или лимфы).
ОНКОТИЧЕСКИЙ ФАКТОР
Онкотический (гипоальбуминемический, гипопротеинемический) фактор развития отёка включается при снижении онкотического давления крови и увеличении его в межклеточной жидкости. Причины развития онкотического отёка.
♦ Снижение онкотического давления крови в результате гипопротеинемии (в основном за счёт гипоальбуминемии; альбумины примерно в 2,5 раза более гидрофильны, чем глобулины). Наиболее часто содержание альбуминов уменьшается при недостаточном поступлении или избыточной потере белков, снижении синтеза альбуминов в печени.
♦ Повышение онкотического давления интерстициальной жидкости при деструкции клеток и гидролизе протеинов межклеточной жидкости.
Механизм реализации онкотического фактора заключается в увеличении фильтрации жидкой части крови в капиллярах и уменьшении реабсорбции воды в посткапиллярах и венулах (как следствие гипопротеинемии и гиперонкии ткани).
ОСМОТИЧЕСКИЙ ФАКТОР
Осмотический фактор развития отёка запускается при повышении осмоляльности интерстициальной жидкости и снижении осмоляльности плазмы крови.
Причины развития осмотического отёка.
• Факторы, снижающие осмотическое давление крови и вызывающие развитие гипоосмолярной гипергидратации (см. выше).
• Факторы, повышающие осмоляльность интерстициальной жидкости:
♦ выход из повреждённых и разрушенных клеток осмотически активных веществ (ионов Na+, K+, Ca2+, глюкозы, МК, азотистых соединений);
♦ повышение диссоциации в интерстициальной жидкости солей и органических соединений (например, в условиях гипоксии или ацидоза);
♦ снижение транспорта осмотически активных веществ (ионов, органических и неорганических соединений) от тканей в результате замедления оттока крови по венулам;
♦ транспорт Na+ из плазмы крови в интерстициальную жидкость (например, при гиперальдостеронизме).
Механизм образования осмотического отёка заключается в избыточном транспорте воды из крови в межклеточную жидкость по градиенту осмотического давления. Данный механизм имеет место при сердечном, почечном (нефритическом), печёночном и ряде других отёков.
МЕМБРАНОГЕННЫЙ ФАКТОР
Мембраногенный фактор характеризуется существенным повышением проницаемости стенок сосудов микроциркуляторного русла для воды, мелко- и крупномолекулярных веществ.
Причины повышения проницаемости сосудистых стенок: ацидоз, активация гидролитических ферментов, перерастяжение стенок сосуда, изменение формы клеток эндотелия. Механизмы реализации мембраногенного фактора:
♦ облегчение фильтрации воды из крови в интерстициальное пространство. Этот механизм может быть сбалансирован повышением реабсорбции воды в посткапиллярах в связи с истончением их стенок;
♦ увеличение выхода молекул белка из плазмы крови в межклеточную жидкость ведёт к включению онкотического фактора. Такой механизм лежит в основе развития отёка при воспалении, местных аллергических реакциях, укусах насекомых и змей.
МНОГОФАКТОРНОСТЬ
В клинической практике, как правило, не встречаются монопатогенетические отёки (развивающиеся на основе только одного из описанных выше патогенетических факторов). В каждом конкретном случае в патогенезе отёка выделяют: 1) инициальный (стартовый, первичный) патогенетический фактор и 2) вторичные патогенетические факторы, включающиеся по ходу развития отёка, особенно при его хроническом течении.
Клинические варианты отёков ОТЁКИ ПРИ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ
Причина: сердечная недостаточность (состояние, при котором сердце не может адекватно обеспечить потребности органов и тканей в кровоснабжении).
Патогенез
Инициальный патогенетический фактор — гидродинамический.
• Последовательность включения и значимость других, указанных ниже, патогенетических факторов отёка могут быть различными в зависимости от динамики расстройств кровообращения и их последствий. К числу основных относятся: Уменьшение кровотока в сосудах почек.
♦ Причина: снижение величины минутного объёма кровотока.
♦ Механизм реализации: активация системы «ренин-ангиотензинальдостерон», вследствие чего усиливается реабсорбция Na+ в канальцах почек.
• Увеличение синтеза АДГ (гидродинамический фактор патогенеза отёка).
♦ Причина: увеличение реабсорбции Na+ в почках.
♦ Механизм реализации: гиперосмия крови (за счёт увеличения концентрации Na+) приводит к активации осморецепторов, усилению синтеза и высвобождения в кровь АДГ. Под влиянием этого гормона в почках увеличивается реабсорбция воды, что приводит к гиперволемии и включению гидродинамического фактора.
• Развитие механической лимфатической недостаточности (лимфогенный фактор).
♦ Причина: увеличение центрального венозного давления вследствие ослабления насосной функции сердца.
♦ Механизм реализации: торможение оттока лимфы из лимфатических протоков в венозную систему приводит к развитию механической лимфатической недостаточности (лимфогенный фактор).
• Увеличение осмотического давления в тканях (осмотический фактор патогенеза).
♦ Причины: венозный застой и лимфатическая недостаточность, изменение метаболизма в условиях гипоксии.
♦ Механизм реализации: увеличение образования метаболитов и снижение транспорта осмотически активных веществ от тканей приводит к повышению осмотического давления в интерстициальной жидкости и включению осмотического фактора.
• Повышение проницаемости сосудистой стенки (мембраногенный фактор).
♦ Причина: перерастяжение сосудов в условиях гиперволемии.
♦ Механизм реализации: облегчение фильтрации воды и повышение выхода белка из крови в интерстициальное пространство.
• Развитие печёночной недостаточности (онкотический фактор патогенеза).
♦ Причина: нарушение кровоснабжения печени.
♦ Механизмы реализации: расстройства энергетического, субстратного и кислородного обеспечения синтеза белка в гепатоцитах приводит к развитию гипоальбуминемии и включению онкотического фактора.
Таким образом, развитие отёка при сердечной недостаточности является результатом сочетанного и взаимопотенцирующего действия всех патогенетических факторов: гидродинамического, осмотического, онкотического, мембраногенного и лимфогенного.
ОТЁК ЛЁГКИХ
Как правило, отёк лёгких развивается весьма быстро. В связи с этим он чреват острой общей гипоксией и существенными расстройствами КЩР.
Причины
• Острая сердечная недостаточность (левожелудочковая или общая).
• Токсичные вещества, повышающие проницаемость стенок сосудов лёгких (например, фосген, фосфорорганические соединения, угарный газ, чистый кислород под высоким давлением).
Механизм развития
• Механизм развития отёка лёгких при сердечной недостаточности.
♦ Инициальный и основной патогенетический фактор — гемодинамический. При снижении сократительной функции миокарда левого желудочка кровь застаивается в сосудах малого круга кровообращения. При увеличении давления выше 25-30 мм рт.ст. вода начинает поступать в межклеточное пространство лёгких (развивается интерстициальный отёк).
♦ При накоплении в интерстиции большого количества отёчной жидкости она проникает между клетками эпителия альвеол, заполняя полости последних (развивается альвеолярный отёк). В связи с этим нарушается газообмен в лёгких, развиваются дыхательная гипоксия и ацидоз.
• Отёк лёгких при действии токсичных веществ. Инициальный и основной патогенетический фактор — мембраногенный. Под воздействием чистого кислорода или токсичных веществ увеличивается проницаемость стенок сосудов и изменяется форма эндотелия капилляров малого круга кровообращения.
ПОЧЕЧНЫЕ ОТЁКИ
Заболевания почек часто сопровождаются развитием отёчного синдрома. Патогенетические звенья образования отёков различны при нефритическом и нефротическом синдромах.
Отёк при нефротическом синдроме
Нефротический синдром развивается при патологии почек, как правило, первично невоспалительного генеза.
Инициальный патогенетический фактор отёка — онкотический.
• Причина отёка — потеря белка с мочой. Протеинурия (при нефротическом синдроме она может достигать 35-55 г в сутки) является следствием:
♦ Повышения проницаемости мембран почечных клубочков для белка, что сопровождается потерей не только альбуминов, но и глобулинов (трансферрина, гаптоглобина, церулоплазмина).
♦ Нарушения реабсорбции белков в канальцах почек.
• Звенья патогенеза:
♦ Снижение концентрации белка в плазме крови (гипопротеинемия) до 20-25 г/л (при норме 65-85 г/л).
♦ Увеличение фильтрации воды в капиллярах и накопление её избытка в межклеточном пространстве и полостях тела (онкотический фактор).
♦ Уменьшение эффективной онкотической всасывающей силы в посткапиллярах и венулах.
♦ Сдавление лимфатических сосудов отёчной тканью с развитием механической лимфатической недостаточности (лимфогенный фактор).
♦ Уменьшение ОЦК (гиповолемия).
♦ Снижение кровотока в почках (вызванное гиповолемией), активирует систему «ренин-ангиотензин-альдостерон». Это потенцирует реабсорбцию Na+ в почках.
♦ Увеличение [Na+] в плазме крови (гипернатриемия), приводящее к активации осморецепторов, усилению синтеза и высвобождения в кровь АДГ.
♦ Активация реабсорбции воды в канальцах почек.
♦ Увеличение эффективного гидростатического давления вследствие сдавления отёчной тканью венул, включающее гидростатический фактор.
Таким образом, в развитии нефротического отёка принимают участие преимущественно онкотический, гидростатический и лимфогенный факторы.
Отёк при нефритическом синдроме
Нефритический синдром развивается при заболеваниях почек первично воспалительного генеза.
Инициальный и основной патогенетический фактор — гидростатический.
• Причина отёка: нарушение кровоснабжения почек вследствие сдавления почечных сосудов экссудатом при воспалительных заболеваниях (например, при гломерулонефрите).
• Звенья патогенеза:
♦ Снижение кровотока в капиллярах клубочков приводит к уменьшению клубочковой фильтрации. Вследствие этого из плазмы крови выводится меньшее количество воды, чем в норме. Это вызывает увеличение ОЦК и включение гидродинамического фактора.
♦ Ишемия клеток юкстагломерулярного аппарата, приводящая к усилению синтеза и выделения в кровь ренина.
♦ Образование в крови под влиянием ренина ангиотензина I, который при участии ангиотензин-превращающего фермента (АПФ)
трансформируется в ангиотензин II. Этот процесс происходит в стенках сосудов (преимущественно в лёгких).
♦ Стимуляция ангиотензином II выделения клетками клубочковой зоны коры надпочечников альдостерона.
♦ Увеличение реабсорбции Na+ в канальцах почки с развитием гипернатриемии.
♦ Активация осморефлекса, сопровождающаяся выделением в кровь АДГ.
♦ Возрастание реабсорбции воды в канальцах почек с развитием гиперволемии, что способствует реализации гидростатического фактора.
В патогенезе нефритического отёка, помимо указанных выше, также могут принимать участие онкотический (при появлении протеинурии) и мембраногенный (при гломерулонефрите часто развивается генерализованный капилляриит) факторы.
Патогенная и адаптивная роль отёков
Патогенная роль отёков
• Механическое сдавление тканей.
♦ Обусловливает нарушение крово- и лимфооттока в результате сдавления сосудов.
♦ Вызывает болевые ощущения в связи с растяжением и смещением участков тканей и расположенных в них нервных окончаний.
• Нарушение обмена веществ между кровью и клетками с развитием различных дистрофий.
• Избыточный рост клеточных и неклеточных элементов соединительной ткани в зоне отёка с развитием склероза.
• Частое развитие инфекций в отёчной ткани. Механизм: подавление активности иммунных механизмов и факторов неспецифической защиты системы ИБН в условиях гипоксии и нарушения метаболизма.
• Нервно-психические расстройства (при отёке мозга).
• Расстройства КЩР вследствие образования избытка кислых продуктов анаэробного гликолиза при гипоксии.
• Нарушение функций жизненно важных органов, чреватых смертью пациента. Так, отёк мозга, лёгких, почек, гидроперикардиум, гидроторакс могут привести к смерти больного.
Адаптивная роль отёков
Адаптивное значение отдельных реакций и процессов, наблюдающихся при развитии отёков, состоит в следующем.
• Уменьшение содержания в крови веществ, оказывающих патогенное действие на ткани, в связи с их транспортом из сосудов в отёч-
ную жидкость (например, продуктов нормального и нарушенного метаболизма, токсинов при почечных и печёночном отёках).
• Снижение концентрации в отёчной ткани токсичных веществ, повреждающих клетки (например, при аллергических, воспалительных, токсических отёках) в результате разбавления токсичных веществ отёчной жидкостью.
• Предотвращение распространения токсичных веществ по организму из зоны повреждения. Отёчная жидкость сдавливает лимфатические и венозные сосуды, снижая тем самым степень распространения с кровью по ткани, органу и организму патогенных агентов: токсинов, продуктов метаболизма, микроорганизмов.
Принципы и методы устранения отёков
Мероприятия, направленные на ликвидацию или уменьшение степени отёков, базируются на этиотропном, патогенетическом и симптоматическом принципах лечения.
• Этиотропный принцип. Имеет целью устранение причины и условий, способствующих возникновению отёка (например, заболеваний почек, печени; лечение сердечной недостаточности, проведение дезинтоксикационной терапии).
• Патогенетический принцип. Направлен на блокирование инициального, а также вторичных звеньев механизма развития отёка.
• Симптоматический принцип. Имеет целью устранение патологических процессов, симптомов и реакций, утяжеляющих состояние пациента: уменьшение степени гипоксии при отёке лёгких; ликвидация асцита при сердечной недостаточности или портальной гипертензии; удаление избытка отёчной жидкости из плевральной или суставных полостей.
Источник
