Механизм франка старлинга в патогенезе сердечных отеков
Согласно классической теории Э. Старлинга (1896), нарушение обмена воды между капиллярами и тканями определяется следующими факторами: 1) гидростатическим давлением крови в капиллярах и давлением межтканевой жидкости; 2) коллоидноосмотическим давлением плазмы крови и тканевой жидкости; 3) проницаемостью капиллярной стенки.
Кровь движется в капиллярах с определенной скоростью и под определенным давлением (рис. 12-45), в результате чего создаются гидростатические силы, стремящиеся вывести воду из капилляров в интерстициальное пространство. Эффект гидростатических сил будет тем больше, чем выше кровяное давление и чем меньше величина давления тканевой жидкости. Гидростатическое давление крови в артериальном конце капилляра кожи человека составляет 30-32 мм рт.ст., а в венозном конце — 8-10 мм рт.ст.
Установлено, что давление тканевой жидкости является величиной отрицательной. Она на 6-7 мм рт.ст. ниже величины атмосферного давления и, следовательно, обладая присасывающим эффектом действия, способствует переходу воды из сосудов в межтканевое пространство.
Таким образом, в артериальном конце капилляров создается эффективное гидростатическое давление(ЭГД) — разность между гидростатическим давлением крови и гидростатическим давлением межклеточной жидкости, равное ~ 36 мм рт.ст. (30 — (-6)). В венозном конце капилляра величина ЭГД соответствует 14 мм рт.ст.
(8 — (-6)).
Удерживают воду в сосудах белки, концентрация которых в плазме крови (60-80 г/л) создает коллоидно-осмотическое давление, равное 25-28 мм рт.ст. Определенное количество белков содержится в межтканевых жидкостях. Коллоидно-осмотическое
Обмен жидкости между различными частями капилляра и тканью (по Э. Старлингу): pa — нормальный перепад гидростатического давления между артериальным (30 мм рт.ст.) и венозным (8 мм рт.ст.) концом капилляра; bc — нормальная величина онкотического давления крови (28 мм рт.ст.). Влево от точки A (участок Ab) происходит выход жидкости из капилляра в окружающие ткани, вправо от точки А (участок Ac) происходит ток жидкости из ткани в капилляр (А1 — точка равновесия). При повышении гидростатического давления (p’a’) или снижении онкотического давления (b’c’) точка A смещается в положение А1 и А2. В этих случаях переход жидкости из ткани в капилляр затрудняется и возникает отек
давление интерстициальной жидкости для большинства тканей составляет ~ 5 мм рт.ст. Белки плазмы крови удерживают воду в сосудах, белки тканевой жидкости — в тканях. Эффективная онкотическая всасывающая сила(ЭОВС) — разность между величиной коллоидно-осмотического давления крови и межтканевой жидкости. Она составляет ~ 23 мм рт. ст. (28-5). Если эта сила превышает величину эффективного гидростатического давления, то жидкость будет перемещаться из интерстициального пространства в сосуды. Если ЭОВС меньше ЭГД, обеспечивается процесс ультрафильтрации жидкости из сосуда в ткань. При выравнивании величин ЭОВС и ЭГД возникает точка равновесия А (см. рис. 12-45).
В артериальном конце капилляров (ЭГД = 36 мм рт.ст., а ЭОВС = 23 мм рт.ст.) сила фильтрации преобладает над эффективной онкотической всасывающей силой на 13 мм рт.ст. (36-23). В точке равновесия А эти силы выравниваются и составляют 23 мм рт.ст. В венозном конце капилляра ЭОВС превосходит эффективное гидростатическое давление на 9 мм рт.ст. (14 — 23 = -9), что определяет переход жидкости из межклеточного пространства в сосуд.
По Э. Старлингу, имеет место равновесие: количество жидкости, покидающей сосуд в артериальной части капилляра, должно быть равно количеству жидкости, возвращающейся в сосуд в венозном конце капилляра. Как показывают расчеты, такого равновесия не происходит: сила фильтрации в артериальном конце капилляра равна 13 мм рт.ст., а всасывающая сила в венозном конце капилляра -9 мм рт.ст. Это должно приводить к тому, что в каждую единицу времени через артериальную часть капилляра в окружающие ткани жидкости выходит больше, чем возвращается обратно. Так оно и происходит — за сутки из кровяного русла в межклеточное пространство переходит около 20 л жидкости, а обратно через сосудистую стенку возвращается только 17 л. Три литра транспортируется в общий кровоток через лимфатическую систему. Это довольно существенный механизм возврата жидкости в кровяное русло, при повреждении которого могут возникать так называемые лимфатические отеки.
Источник
Преднагрузка и постнагрузка на сердце. Механизм Франка-Старлинга
Оценивая сократительные свойства мышцы, очень важно определить степень напряжения мышцы перед началом сокращения (так называемую преднагрузку), а также нагрузку, которую мышце предстоит преодолеть, развивая сокращение (так называемую постнагрузку).
Для сердца преднагрузка определяется величиной конечно-диастолического давления, когда наполнение желудочков кровью завершилось.
Постнагрузка желудочка определяется величиной давления в артерии, берущей начало от данного желудочка. На рисунке это соответствует систолическому давлению во время фазы III диаграммы «объем-давление». (Иногда постнагрузка несколько вольно определяется как сосудистое сопротивление, а не давление в сосудах.)
Понятия преднагрузки и постнагрузки имеют большое практическое значение: нарушение функции сердечно-сосудистой системы может протекать с резкими изменениями как преднагрузки или постнагрузки, так и обоих этих факторов одновременно.
Потребление кислорода сердцем. Сердечная мышца, так же как и скелетная мышца, использует химическую энергию для сократительной деятельности. Энергия освобождается главным образом при окислении жирных кислот и в меньшей степени — при окислении других субстратов, таких как лактат и глюкоза. Таким образом, уровень потребления кислорода сердечной мышцей является основным показателем энергетического обеспечения деятельности сердца.
Эффективность сердечных сокращений. В процессе сокращения сердечной мышцы большая часть освободившейся химической энергии превращается в тепло, а меньшая часть энергии затрачивается на совершение работы. Отношение рабочих энерготрат к общему количеству выделенной энергии характеризует эффективность сердечных сокращений, или коэффициент полезного действия сердца. КПД сердца здоровых людей составляет примерно 20-25%. В случае сердечной недостаточности этот показатель может уменьшаться до 5-10%.
В условиях покоя сердце перекачивает от 4 до 6 л крови в минуту. При тяжелой физической нагрузке сердцу необходимо перекачивать в 4-7 раз больше крови, чем в покое. Такому усилению сердечной деятельности способствуют: (1) внутрисердечные механизмы, регулирующие насосную функцию в зависимости от объема притекающей к сердцу крови; (2) центральные нервные механизмы, контролирующие частоту и силу сердечных сокращений с участием автономной (вегетативной) нервной системы.

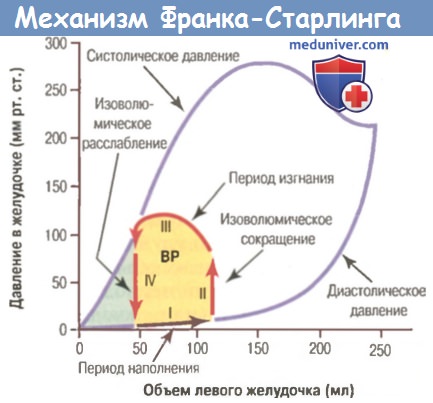
Связь между объемом левого желудочка и внутрижелудочковым давлением во время диастолы и систолы называемтся механизмом Франка-Старлинга.
Красными стрелками показана рабочая диаграмма «объем-давление» (изменение внутрижелудочкового объема и давления в течение сердечного цикла).
ВР — внешняя работа
Механизм Франка-Старлинга
Нам известно, что в разных ситуациях объем крови, который сердце перекачивает за минуту, почти полностью определяется венозным возвратом, т.е. объемом крови, поступающим в сердце из вен. Это можно объяснить следующим образом: кровоток каждого отдельного органа контролируется местными механизмами в зависимости от метаболических потребностей данного органа; кровь, оттекающая от отдельных органов, сливается в общую венозную систему и поступает к сердцу; сердце, в свою очередь, автоматически перекачивает всю поступившую к нему кровь в артериальное русло, снабжая периферические органы, и т.д.
Способность сердца адаптироваться к увеличению объема поступающей к нему крови называют внутрисердечным механизмом Франка—Старлинга, названным в честь выдающихся физиологов прошлого века. Суть механизма в следующем: чем больше степень растяжения миокарда объемом притекающей крови, тем больше сила сокращения сердечной мышцы и, следовательно, тем больше объем крови, который сердце перекачивает в аорту. Другими словами, в физиологических пределах сердце перекачивает всю кровь, которая возвращается к нему по венам.
Как объяснить механизм Франка-Старлинга? Когда избыточный объем крови поступает в желудочки, волокна сердечной мышцы растягиваются. Нити актина и миозина в миофибриллах занимают положение, близкое к оптимальному для развития большей силы сокращения. Таким образом, желудочки автоматически перекачивают избыточный объем крови в артерии.
Способность мышечных волокон, растянутых до оптимальной длины, сокращаться с большей эффективностью характерна для всех поперечнополосатых мышц, а не только для миокарда.
Усиление насосной функции сердца при увеличении венозного возврата происходит и по другой причине. Растяжение стенки правого предсердия приводит к увеличению частоты сердечных сокращений на 10-20%, что тоже вносит вклад в увеличение выброса крови из желудочков в артерии.
— Также рекомендуем «Внешняя регуляция насосной функции сердца. Вегетативная регуляция сердца»
Оглавление темы «Сердечная мышца. Сократительная функция мышцы сердца»:
1. Сердечная мышца. Физиология сердечной мышцы
2. Потенциал действия сердечной мышцы. Скорость проведения импульса в сердечной мышце
3. Связь между возбуждением и сокращением сердца. Роль ионов кальция в сокращении сердца
4. Сердечный цикл. Связь электрокардиограммы и сердечного цикла
5. Насосная функция желудочков. Функции желудочков сердца
6. Функция и физиология клапанов сердца. Кривая аортального давления
7. Насосная функция сердца. Оценка насосной функции сердца
8. Преднагрузка и постнагрузка на сердце. Механизм Франка-Старлинга
9. Внешняя регуляция насосной функции сердца. Вегетативная регуляция сердца
10. Влияние калия и кальция на сердце. Влияние температуры тела на сердце
Источник
Отеки
представляют собой нарушение равновесия
в обмене воды между кровью, тканевой
жидкостью и лимфой. Причины
возникновения и развития отеков можно
разбить на
две группы:
отеки, вызванные изменением факторов,
определяющих местный баланс воды и
электролитов и вторая группа — отеки,
обусловленные регуляторными и почечными
механизмами, приводящими к задержке
натрия и воды в организме.
Скопление
внеклеточной жидкости в полостях тела
получило название водянки.
Различают следующие виды водянок:
водянка брюшной полости – асцит; водянка
плевральной полости – гидроторакс;
водянка полости перикарда – гидроперикард;
водянка желудочков мозга – гидроцефалия;
водянка оболочек яичка – гидроцеле.
В
развитии отеков принимают участие
шесть
основных патогенетических факторов.
1.
Гидродинамический.
На уровне капилляров обмен жидкости
между сосудистым руслом и тканями
осуществляется следующим образом. В
артериальной части капилляров давление
жидкости внутри сосуда превышает ее
давление в тканях, и поэтому здесь
жидкость идет из сосудистого русла в
ткань. В венозной части капилляров
имеются обратные соотношения: в ткани
давление жидкости выше и жидкость идет
из ткани в сосуды. В норме в этих
перемещениях устанавливается равновесие,
которое в условиях патологии может
нарушаться. Если повысится давление в
артериальной части капилляров, то
жидкость начнет интенсивнее переходить
из сосудистого русла в ткани, а если
такое повышение давления будет
происходить в венозной части капиллярного
русла, то это будет препятствовать
переходу жидкости из ткани в сосуды.
Повышение давления в артериальной
части капилляров встречается крайне
редко и может быть связано с общим
увеличением объема циркулирующей
крови. Повышение же давления в венозной
части бывает в условиях патологии
достаточно часто, например, при венозной
гиперемии, при общем венозном застое,
связанном с сердечной недостаточностью.
В этих случаях жидкость задерживается
в тканях и развивается отек, в основе
которого лежит гидродинамический
механизм.
2.
Мембранный.
Этот фактор связан с повышением
проницаемости сосудисто-тканевых
мембран, поскольку в данном случае
облегчается циркуляция жидкости между
кровеносным руслом и тканями. Повышение
проницаемости мембран может наступать
под влиянием биологически активных
веществ (например, гистамина), при
накоплении в тканях недоокисленных
продуктов обмена веществ, при действии
токсических факторов (ионов хлора,
азотнокислого серебра и др.). Частой
причиной развития отеков, в основе
которых лежит мембранный фактор,
являются микробы, выделяющие фермент
гиалуронидазу, который, воздействуя
на гиалуроновую кислоту, ведет к
деполимеризации мукополисахаридов
клеточных мембран и вызывает повышение
их проницаемости.
3.
Осмотический.
Накопление в межклеточных пространствах
и полостях тела электролитов ведет к
повышению в этих областях осмотического
давления, что вызывает приток воды.
4.
Онкотический.
При некоторых патологических состояниях
онкотическое давление в тканях может
становиться большим, нежели в сосудистом
русле. В таком случае жидкость будет
стремиться из сосудистой системы в
ткани, и разовьется отек. Это происходит
либо в случае повышения концентрации
крупномолекулярных продуктов в тканях,
либо в случае снижения содержания белка
в плазме крови.
5.
Лимфатический.
Этот фактор играет роль в развитии
отека в тех случаях, когда в органе
наступает застой лимфы. При повышении
давления в лимфатической системе вода
из нее идет в ткани, что и приводит к
отеку.
6. В
числе факторов, способствующих развитию
отека, выделяют также снижение
тканевого механического давления,
когда уменьшается механическое
сопротивление току жидкости из сосудов
в ткани, как, например, при обеднении
тканей коллагеном, повышении их рыхлости
при усилении активности гиалуронидазы,
что наблюдается, в частности, при
воспалительных и токсических отеках.
Таковы
основные патогенетические механизмы
развития отеков. Однако «в чистом виде»
монопатогенетические отеки встречаются
очень редко, обычно рассмотренные выше
факторы комбинируются. нка желудочков
мозга – гидроцефалия.
Транскапиллярный
обмен (ТКО)
– это процессы движения веществ (воды
и
растворенных в ней солей, газов,
аминокислот, глюкозы шлаков и др.) через
стенку
капилляра из крови в интерстициальную
жидкость и из интерстициаль-
ной
жидкости в кровь, это связывающее звено
перемещения веществ между
кровью
и клетками.
Механизм
транскапиллярного обмена включает
процессы фильтрации,
реабсорбции
и диффузии.
Принципиальные
закономерности фильтрации и реабсорбции
жидкостей
при ТКО
отражает формула
Старлинга:
ТКО
= К [(ГДК – ГДИ) – (КОДК – КОДИ)]
или
ТКО
= К (∆ГД- ∆КОД).
В
формулах:
К –
константа проницаемости стенки
капилляров;
ГДК
– гидростатическое давление в капиллярах;
ГДИ
– гидростатическое давление в
интерстиции;
КОДК
– коллоидно-осмолярное давление в
капиллярах;
КОДИ
— коллоидно-осмолярное давление в
интерстции;
∆ГД
– разница гидростатического
внутрикапиллярного и интестициально-
го
давлений;
∆КОД
– разница коллоидно-осмолярного
внутрикапилярного и интерсти-
циального
давлений.
В
артериальной и венозной частях
капиллярного русла эти факторы ТКО
имеют различное значение.
Величина
константы проницаемости (К) определяется
функциональным состоянием организма,
его обеспеченностью витаминами,
действием гормонов, вазоактивных
веществ, факторов интоксикации и пр.
При
движении крови через капилляры в
артериальной части капиллярного русла
преобладают силы гидростатического
внутрикапиллярного давления, что
вызывает фильтрацию жидкости из
капилляров в интерстиций и к клеткам;
в венозной части капиллярного русла
преобладают силы внутрикапиллярного
КОД, что вызывает реабсорбцию жидкости
из интерстиция и от клеток в капилляры.
Силы фильтрации и реабсорбции и,
соответственно, объемы фильтрации и
реабсорбции равны. Так, рассчеты по
формуле Стерлинга показывают, что в
артериальной части капиллярного русла
силы фильтрации равны:
ТКО
= К [(30-8)- (25-10)] = +К 7 (мм рт.ст.);
в
венозной части капиллярного русла силы
реабсорбции равны:
ТКО
= К[(15-8) — (25-11)] = -К 7 (мм рт.ст.).
Приведены
лишь принципиальные сведения о ТКО. В
действительности имеется небольшое
преобладание фильтрации над реабсорбцией.
Однако отека тканей не возникает, так
как в транскапиллярном обмене жидкостей
участвует и отток жидкостей по
лимфатическим капиллярам (рис. 3). При
неполноценности дренирующей функции
лимфатических сосудов отек тканей
возникает даже при небольшом нарушении
сил ТКО. В транскапиллярном обмене
участвуют и процессы диффузии электролитов
и неэлектролитов через стенки капилляров,
то есть процессы их проникновения через
капиллярную стенку в силу различия
градиентов концентрации и их различной
способности к проникновению (см. ниже).
В более полном виде закономерности ТКО
обмена могут быть представлены в виде
следующей формулы.
ТКО
= К (∆ГД — Д Ч ∆КОД) — Лимфоток,
где
символом Д обозначены процессы диффузии
и отражения макромолекул от стенки
капилляра.
Изменения
проницаемости капилляров, гидростатических
и коллоидно-осмотических давлений
вызывают соответствующие изменения и
ТКО. В механизмах ТКО особенно важную
роль, как уже ранее указывалось, играют
белки плазмы — альбумины, глобулины,
фибриноген и др., создающий КОД. Величина
КОД плазмы (25 мм рт. ст.) на 80-85% обеспечивается
альбуминами, на 16-18% глобулинами и
примерно на 2% белками свертывающей
системы крови. Альбумины обладают
наибольшей водоудерживающей функцией:
1 г альбумина удерживает 18-20 мл воды, 1
г глобулинов — только 7мл. Все белки
плазмы в целом удерживают примерно 93%
внутрисосудистой жидкости. Критический
уровень содержания белка в плазме
зависит от профиля протеинограммы и
ориентировочно равен 40-50 г/л. Снижение
ниже этого уровня (особенно в случаях
преобладающего снижения альбуминов)
вызывает гипопротеинемические отеки,
ведет к уменьшению ОЦК, исключает
возможность эффективного репаративного
восстановления объема крови после
кровопотери.
Учет
закономерностей Старлинга в практической
работе во многих случаях является
основой построения терапии, адекватной
патологическому состоянию. Закономерности
Старлинга патогенетически объясняют
важнейшие проявления всех заболеваний,
связанных с нарушениями водно-солевого
обмена и гемодинамики, обеспечивают
правильный выбор необходимой терапии.
В
частности, они раскрывают механизм
отека легких при гипертоническом кризе
и при сердечной недостаточности,
механизм репаративного притока
интерстициальной жидкости в сосудистое
русло при кровопотере, причину развития
отечно-асцитического синдрома при
тяжелых гипопротеинемиях. Эти же
закономерности обосновывают
патогенетическую адекватность применения
для лечения отека легких нитритов,
ганглиоблокаторов, кровопусканий,
наложения жгутов на конечности, морфина,
ИВЛ с положительным давлением в конце
вдоха, фторотанового наркоза и пр.,
объясняют категорическую недопустимость
применения в лечении отека легких
инфузий осмодиуретиков (маннитола и
др.), обосновывают необходимость
коллоидно-кристаллоидных препаратов
при лечении шока и кровопотери, их
объемы и схемы применения.
Как уже
было указано выше, кроме процессов
фильтрации и реабсорбции в механизмах
ТКО большое значение имеют процессы
диффузии. Диффузия – это перемещение
растворенных веществ через разделяющую
проницаемую мембрану или в самом
растворе из зоны с высокой концентрацией
вещества в зону с низкой концентрацией.
При ТКО диффузия постоянно поддерживается
разностью концентраций веществ по обе
стороны проницаемой капиллярной
мембраны. Эта разность непрерывно
возникает в ходе обмена веществ и
движения жидкостей. Интенсивность
диффузии зависит от константы
проницаемости капиллярной мембраны и
от свойств диффундирующего вещества.
Диффузия веществ из интерстиция в
клетки и из клеток в интерстиций
определяет обмен веществ между клетками.
Соседние файлы в предмете Патологическая физиология
- #
11.09.201687.88 Mб288Адо. Патологическая физиология (2000).pdf
- #
- #
- #
- #
- #
- #
Источник
