Как передается по наследству отек квинке

Согласно медицинской статике, примерно 10-20% населения планеты хотя бы раз в жизни сталкивается с таким состоянием, как отек Квинке, или ангионевротический отек. В большей части случаев он является симптомом аллергии и сочетается с высыпаниями на коже — крапивницей. Однако иногда отек Квинке — проявление наследственного заболевания, которое требует специфического лечения. MedAboutMe расскажет, в чем принципиальные отличия.
Отек Квинке как симптом аллергии

Отек Квинке — острое состояние, которое проявляется безболезненным отеком кожи и слизистых оболочек. Чаще всего он развивается в области лица и шеи, но может возникнуть в любой другой части тела, включая кишечник. Обычно проходит самостоятельно в течение 2-3 дней. Наиболее грозным осложнением ангионевротического отека является обструкция дыхательных путей, иными словами, невозможность сделать вдох и выдох из-за отека слизистой гортани или языка.
В 50% случаев отек Квинке является симптомом аллергии и сопровождает острую крапивницу — «летучие» и сильно зудящие красные высыпания на теле. Реакция появляется быстро после контакта с аллергеном. Наиболее частыми причинами становятся: употребление пищевых продуктов, прием некоторых лекарственных препаратов, укусы насекомых, вдыхание пыльцы растений.
Многие хорошо известные симптомы аллергии, в том числе крапивница и отек Квинке, возникают в результате выброса из тучных клеток уже готовых веществ: гистамина, лейкотриенов и простагландинов. Они приводят к расширению сосудов и «пропотеванию» жидкости в ткани, что визуально проявляется отеком.
Наследственный ангиневротический отек

Наследственный ангионевротический отек — редкое генетическое заболевание. По сути, он относится к первичному или врожденному иммунодефициту, который затрагивает одно из звеньев иммунитета — систему комплимента.
Согласно статистическим данным заболевание развивается в 1 случае на 50 000—150 000 человек. При этом шанс рождения больного ребенка равен 50%, если один из родителей страдает от наследственного ангионевротического отека. Одинаково часто болеют как мужчины, так и женщины.
Считается, что течение наследственного ангионевротического отека непредсказуемо. Однако некоторые закономерности все же можно выделить. Как правило, болезнь дебютирует у детей от 7 до 15 лет и продолжается в течение всей жизни с некоторым уменьшением выраженности симптомов в старшем возрасте. Без соответствующего лечения обострения в среднем возникают каждые 2 недели. Выявлен определенный перечень факторов, провоцирующих ухудшение состояния:
- Психологический фактор: эмоциональный стресс;
- Травма: даже минимальное повреждение тканей, например, слизистой полости рта;
- Изменение гормонального фона: менструация, беременность;
- Инфекции верхних дыхательных путей.
Наследственный ангионевротический отек имеет отличный от симптомов аллергии механизм развития, что определяет неэффективность традиционной схемы лечения. Он связан с активацией системы комплимента и увеличением уровня брадикинина, а также недостатком С1-ингибитора.
Отличить симптомы аллергии от проявлений наследственного ангионевротического отека — непростая задача. Порой с момента начала болезни и до постановки верного диагноза проходит 20 лет.
Больные, страдающие от наследственного ангионевротического отека, сталкиваются с серьезной проблемой. Несмотря на известный перечень факторов, провоцирующих обострение, предугадать в какой момент случится следующий приступ болезни невозможно, так же, как и область отека, и его тяжесть.
Отличия в лечении отеков
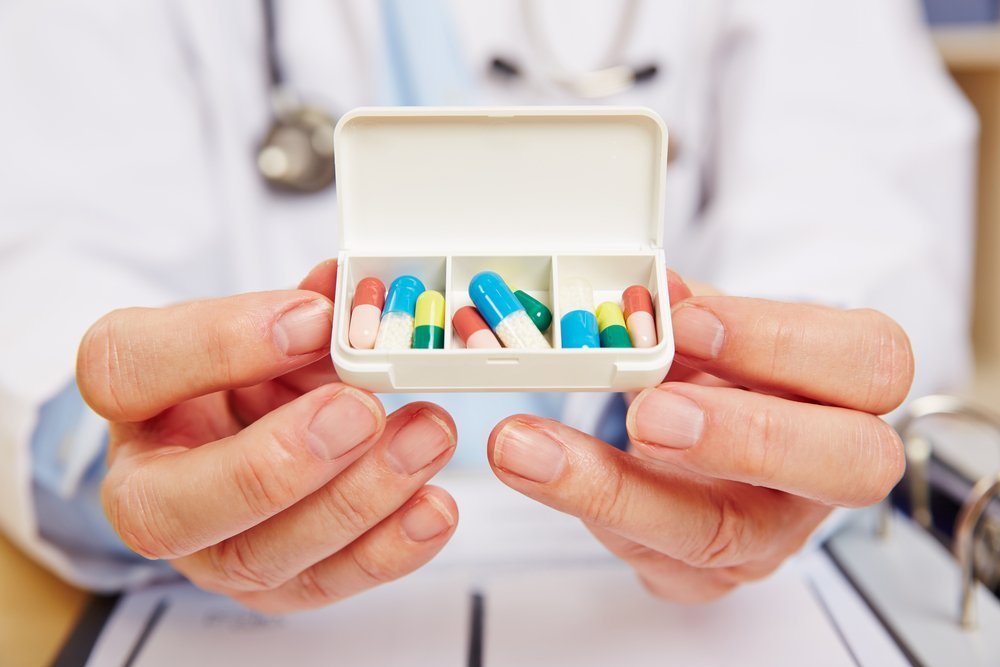
Лечение отеков аллергической природы основано на механизме их развития. Учитывая то, что ведущую роль играет выброс гистамина из тучных клеток после контакта человека с аллергеном, то остановить реакцию могут антигистаминные препараты (цетиризин, лоратадин, фексофенадин и другие). При их неэффективности врач может назначить инъекцию гормонального препарата — глюкокортикостероида (дексаметазона или преднизолона).
В лечении наследственного ангионевротического отека можно выделить три фазы, которые преследуют разные цели:
- Купирование обострения;
- Краткосрочная профилактика;
- Долгосрочная профилактика.
Лечение отеков во время обострения зависит от их расположения и тяжести. Обязательно применение лекарственных препаратов при развитии отека лица, шеи, гортани, а также кишечника (проявляется болью в животе, имитируя картину «острого живота»). Лечения отеков других частей тела (например, кисти или стопы) не требуется, потому что они разрешаются самостоятельно в течение 2-3 дней.
Кратковременная профилактика проводится при планировании каких-либо процедур или хирургических вмешательств в области лица, например, лечение и удаление зубов. Такие манипуляции, по сути, травмируют ткани и могут привести к развитию отека опасной зоны. Препаратом выбора в этом случае является комбинация концентрата С1-ингибитора, свежезамороженной плазмы и Даназола (аттенуированные андрогены). Профилактическое введение препаратов начинают за 24 часа до планируемой процедуры.
Долгосрочная профилактика необходима для снижения частоты, тяжести и длительности обострений наследственного ангионевротического отека. Идеальным результатом такого лечения становится уменьшение частоты обострений до 2 и менее в год. Наиболее эффективными средствами считаются аттенуированные андрогены (Даназол).
Отек Квинке или ангионевротический отек — состояние потенциально опасное, особенно если затрагивает область головы и шеи. В такой ситуации действовать нужно быстро. Однако, к сожалению, не всегда традиционная схема лечения отеков, включающая в себя антигистаминные препараты и глюкокортикостероиды, работает. Несмотря на то, что генетическая патология встречается в разы реже аллергических заболеваний, забывать о ней не стоит. Правильно подобранная терапия и профилактика могут значительно улучшить качество жизни, позволив забыть о страхе внезапного повторения отека.
Источник
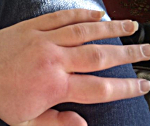
Наследственный ангионевротический отек – генетическое заболевание, при котором наблюдается дефицит ингибитора С1-компонента комплемента. Симптомами являются рецидивирующие отеки кожи, слизистых оболочек и органов брюшной полости, которые могут сопровождаться удушьем (при отеке гортани), рвотой и болями в животе (при поражении брюшной полости). Диагностика производится на основании осмотра, изучения наследственного анамнеза, определения С1-ингибитора, компонентов С4 и С2 в плазме крови, молекулярно-генетических исследований. Лечение осуществляется путем компенсирования абсолютного или функционального дефицита С1-ингибитора, применения блокаторов брадикинина и калликреина, использования свежезамороженной донорской плазмы.
Общие сведения
Наследственный ангионевротический отек (НАО) – вариант первичного иммунодефицита, обусловленный нарушением ингибирования системы комплемента, точнее, его основной фракции С1. Впервые это состояние было описано в 1888 году У. Осиером, который выявил рецидивирующие отеки у молодой женщины, а также установил, что подобное заболевание имелось как минимум у пяти поколений ее семьи. Примечательно, что собственно ангионевротический отек был открыт И. Квинке всего за 6 лет до обнаружения наследственной формы этой патологии – в 1882-м году. Наследственный ангионевротический отек имеет аутосомно-доминантный характер передачи и с одинаковой частотой поражает как мужчин, так и женщин. По некоторым данным, у женщин заболевание протекает тяжелее и возникает раньше, однако достоверных исследований по этому поводу не производилось. Встречаемость наследственного ангионевротического отека, по всей видимости, значительно варьирует у разных этнических групп, что дает весьма неоднородные цифры этого показателя – от 1:10 000 до 1:200 000.
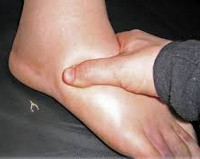
Наследственный ангионевротический отек
Причины наследственного ангионевротического отека
Непосредственной причиной развития наследственного ангионевротического отека является первичный иммунодефицит, заключающийся в дефиците или функциональной неполноценности ингибитора эстеразы одного из компонентов комплемента – С1. В результате этого также нарушается ингибирование активации других компонентов этой системы – С4 и С2, что приводит к еще большему расстройству работы данного иммунного механизма. Врачам-генетикам удалось установить ген, отвечающий за 98% форм наследственного ангионевротического отека – им является C1NH, расположенный на 11-й хромосоме и кодирующий вышеуказанный ингибитор эстеразы С1. Различные мутации способны приводить к неодинаковым по своему течению формам заболевания, которые обладают достаточно сходными клиническими проявлениями, но различаются при проведении ряда диагностических тестов.
При одних типах мутации гена C1NH происходит полное прекращение синтеза белка-ингибитора С1, в результате чего он отсутствует в плазме крови, а остановка системы комплемента производится малоэффективными побочными путями. В других случаях наследственный ангионевротический отек возникает на фоне нормального содержания ингибитора в крови, при этом генетический дефект C1NH приводит к нарушению структуры активного центра данного фермента. В результате ингибитор С1 становится функционально неполноценным, что и служит причиной развития патологии. Существуют также редкие формы наследственного ангионевротического отека, при которых не наблюдается как изменений количества или активности ингибитора эстеразы С1, так и мутаций в гене C1NH – этиология и патогенез таких заболеваний на сегодняшний день неизвестны.
Остановка ингибирования активности компонентов комплемента (С1, С2, С4) приводит к запуску иммунной реакции, сходной по своему течению с аллергической, особенно крапивницей. Компоненты комплемента способны расширять кровеносные сосуды глубоких слоев дермы, повышать проницаемость их стенок, что провоцирует диффундирование компонентов плазмы крови в межклеточное пространство тканей кожи и слизистых оболочек и приводит к их отеку. Кроме того, немаловажную роль в патогенезе наследственного ангионевротического отека играют вазоактивные полипептиды – брадикинин и калликреин, которые еще больше увеличивают степень отека, а также способны вызывать спазм гладкомышечной мускулатуры органов желудочно-кишечного тракта. Эти процессы обуславливают все разнообразие симптомов наследственного ангионевротического отека: отечность кожи (в области конечностей, лица, шеи) и слизистых оболочек (ротовой полости, гортани, глотки), боли в животе и диспепсические расстройства, провоцируемые сочетанием отеков и спазмов.
Классификация наследственного ангионевротического отека
Всего на сегодняшний день выявлено три основных типа наследственного ангионевротического отека. Их различия в плане клинического течения патологии очень незначительны, для определения формы заболевания используют специальные диагностические методики. Врачу-иммунологу крайне важно выяснить тип наследственного ангионевротического отека, так как от этого во многом зависит тактика лечения данной патологии:
- Наследственный ангионевротический отек 1-го типа (НАО-1) – является наиболее распространенной формой заболевания, регистрируется у 80-85% больных с такой патологией. Причиной НАО этого типа является отсутствие гена C1NH или нонсенс-мутация в нем, в результате чего ингибитор С1 не образуется в организме.
- Наследственный ангионевротический отек 2-го типа (НАО-2) – более редкая форма патологии, выявляется лишь у 15% больных. Обусловлен также генетическим дефектом в C1NH, однако при этом экспрессия белка-ингибитора С1 не останавливается, а сам фермент имеет измененную структуру своего активного центра. Это приводит к его неполноценности, и он становится неспособен правильно выполнять свои функции.
- Наследственный ангионевротический отек 3-го типа – относительно недавно обнаруженная форма заболевания с практически неизученными этиологией и патогенезом. Достоверно удалось выяснить, что при этом типе отека отсутствуют мутации гена C1NH, сохраняется нормальное количество ингибитора эстеразы компонента комплемента С1 и его функциональная активность. Больше никаких данных по поводу данной формы (или их совокупности) наследственного ангионевротического отека не имеется.
Симптомы наследственного ангионевротического отека
Как правило, при рождении и в детском возрасте (за исключением редких случаев) наследственный ангионевротический отек ничем себя не проявляет. Довольно часто первые признаки заболевания возникают в подростковом периоде, так как их провоцируют стрессы и гормональные перестройки, происходящие в организме в это время. Однако нередко наследственный ангионевротический отек появляется позже – в возрасте 20-30 лет или даже у пожилых лиц. Чаще всего развитию первого приступа предшествует какое-либо провоцирующее явление: мощный эмоциональный стресс, серьезное заболевание, хирургическое вмешательство, прием некоторых лекарственных средств. В дальнейшем «порог чувствительности» по отношению к провоцирующим факторам снижается, приступы возникают все чаще – наследственный ангионевротический отек приобретает рецидивирующий характер.
Основным проявлением заболевания у большинства больных является отек кожи и подкожной клетчатки на кистях, стопах, иногда лице и шее. В более тяжелых случаях отечные явления возникают на слизистых оболочках полости рта, гортани и глотки – при этом может развиваться удушье (асфиксия), являющееся наиболее частой причиной смерти от наследственного ангионевротического отека. В других случаях на первый план выступают симптомы со стороны желудочно-кишечного тракта: тошнота, рвота, боли и рези в животе, иногда подобная клиническая картина приобретает черты «острого живота». В отдельных случаях наследственный ангионевротический отек характеризуется сочетанием отека кожи, слизистых оболочек и поражения желудочно-кишечного тракта.
Диагностика наследственного ангионевротического отека
Для выявления наследственного ангионевротического отека используют данные физикального осмотра больного, изучения его наследственного анамнеза, определения в крови количества ингибитора С1, а также компонентов комплемента С1, С2, С4, и молекулярно-генетических исследований. Осмотр в фазу обострения заболевания выявляет отек кожи или слизистых оболочек, пациенты могут жаловаться на боли в животе, рвоту, диарею. В крови при наличии наследственного ангионевротического отека 1-го типа ингибитор эстеразы С1 полностью отсутствует, значительно снижены концентрации индикаторных компонентов комплемента. При 2-м типе заболевания в плазме крове может определяться незначительное количество ингибитора С1, в редких случаях его уровень соответствует норме, но соединение имеет пониженную функциональную активность. При всех трех вариантах наследственного ангионевротического отека уровень С1, С2 и С4 не превышает 30-40% от нормы, поэтому этот показатель является ключевым в диагностике данного состояния.
Изучение наследственного анамнеза пациента зачастую обнаруживает наличие подобного заболевания как минимум у нескольких поколений его предков и у других родственников. Однако отсутствие признаков семейного характера патологии не является однозначным критерием, позволяющим исключить наследственный ангионевротический отек – примерно у четверти больных это состояние обусловлено спонтанными мутациями и выявляется впервые в семье. Молекулярно-генетическая диагностика осуществляется путем автоматического секвенирования гена C1NH с целью выявления мутаций. Дифференциальную диагностику следует производить с ангионевротическим отеком аллергического генеза и приобретенными формами дефицита ингибитора С1.
Лечение наследственного ангионевротического отека
Терапию наследственного ангионевротического отека разделяют на два типа – лечение для купирования острого приступа заболевания и профилактический прием препаратов для предупреждения их развития. В случае острого отека Квинке, обусловленного НАО, традиционные противоанафилактические меры (адреналин, стероиды) неэффективны, необходимо использовать нативный или рекомбинантный ингибитор С1, антагонисты брадикинина и калликреина, при их отсутствии показано переливание свежезамороженной плазмы. Начинать такое лечение нужно как можно раньше, в идеале – при самых первых приступах наследственного ангионевротического отека.
Долгосрочная профилактика заболевания производится в тех случаях, когда приступы возникают слишком часто (чаще раза в месяц), если в анамнезе имелись случаи отека гортани или удушья, либо госпитализация в реанимационное отделение. Профилактика включает в себя использование андрогенов, экзогенных (рекомбинантных или нативных) форм ингибитора эстеразы С1, антифибринолитических препаратов. При доброкачественном течении наследственного ангионевротического отека – редких приступах и их относительно быстром исчезновении – такое лечение может не назначаться. Однако накануне хирургических или стоматологических вмешательств, физических и умственных нагрузок рекомендуется краткосрочно принимать вышеуказанные средства для уменьшения риска развития приступа.
Прогноз и профилактика наследственного ангионевротического отека
В большинстве случаев прогноз наследственного ангионевротического отека относительно благоприятный в плане выживаемости – при разумном лечении и профилактике приступы возникают крайне редко и не угрожают жизни больного. При этом всегда сохраняется риск отека гортани, что может привести к асфиксии и летальному исходу. Таким больным следует не только избегать значительных физических и эмоциональных нагрузок, но и желательно иметь при себе карточку или медальон с указанием диагноза. Огромное количество смертей от наследственного ангионевротического отека было обусловлено неверными действиями медиков, не знающих диагноза и поэтому использующих традиционные при аллергическом отеке Квинке препараты, которые неэффективны при НАО.
Источник
Сайт предоставляет справочную информацию. Адекватная диагностика и лечение болезни возможны под наблюдением добросовестного врача. У любых препаратов есть противопоказания. Необходима консультация специалиста, а также подробное изучение инструкции!
Отек Квинке — остро возникающий, безболезненный, отек глубоких слоев кожи и подкожной клетчатки или слизистых оболочек, обусловленный увеличением проницаемости сосудов. В некоторых случаях может приводить к полному закрытию дыхательных путей и смерти.
- Впервые заболевание было описано в 1882 году, немецким врачом и исследователем Генрихом Квинке.
- Более 90% всех случаев отека Квинке и обращений за скорой медицинской помощью связано с применением медикаментов, особенно ингибиторов АПФ (каптоприл, эналаприл).
- Отек Квинке может быть нескольких видов:
- Наследственный отек Квинке
- Приобретенный отек Квинке
- Отек Квинке связанный с аллергическими реакциями (чаще с крапивницей)
- Отек Квинке связанный с приемом медикаментов (чаще у пожилых на ингибиторы АПФ)
- Отек Квинке невыясненной причины (идиопатический)
- Наследственный отек Квинке редкое заболевание развивающиеся лишь у 1 человека из 150 тысяч населения. Впервые было описано в 1888 году у пяти поколений членов американской семьи. Начало эпизодов заболевания чаще регистрируется в возрасте 7-15 лет. У всех пациентов с наследственным отеком Квинке имеется склонность к развитию аутоиммунных заболеваний (системная красная волчанка, аутоиммунный тироидит и др.). Заболевание передается по аутосомно-доминантному типу и шанс рождения ребенка у пары, в которой один родитель болен, равен 50 %.
- Случаи приобретенного отека Квинке достаточно редки за период 1997-2008 года было описано лишь 50 случаев заболевания. Заболевание чаще развивается у людей старше 50 лет.
- Частота развития отека Квинке связанного с применение ингибиторов АПФ составляет 1-2 случая на 1 тыс. населения.
Состояние иммунной системы и механизм развития отека Квинке
 Для понимания причины и механизма возникновения наследственного отека Квинке необходимо разобрать одну из составляющих иммунной системы. Речь пойдет о системе комплимента. Система комплемента – это важный компонент как врожденного, так и приобретенного иммунитета, состоящая из комплекса белковых структур.
Для понимания причины и механизма возникновения наследственного отека Квинке необходимо разобрать одну из составляющих иммунной системы. Речь пойдет о системе комплимента. Система комплемента – это важный компонент как врожденного, так и приобретенного иммунитета, состоящая из комплекса белковых структур.
Система комплемента участвует в реализации иммунного ответа и предназначена для защиты организма от действия чужеродных агентов. Кроме того система комплемента учувствует в воспалительных и аллергических реакциях. Активация системы комплемента приводит к выбросу из специфических иммунных клеток (базофилы, тучные клетки) биологически активных веществ (брадикинина, гистамина, и др.), что в свою очередь стимулирует воспалительную и аллергическую реакцию.
Все это сопровождается расширением сосудов, увеличением их проницаемости для компонентов крови, снижением артериального давления, появлением различных высыпаний и отека. Система комплемента регулируется специфическими ферментами, одним из таких ферментов является ингибитор С1. Количество и качество которого определяет развитие отека Квинке. Научно доказано, что недостаток ингибитора С1, является основной причиной развития наследственного и приобретенного отека Квинке. Исходя из своей функции ингибитор С1 должен сдерживать и контролировать активацию комплемента. Когда его не хватает, происходит неконтролируемая активация комплимента и из специфических клеток (тучные клетки, базофилы), осуществляется массивный выброс биологически активных веществ запускающих механизмы аллергической реакции (брадикинин, серотонин, гистамин и др.). Основной причиной отека является брадикинин и гистамин, которые расширяют сосуды и увеличивают проницаемость сосудов для жидкой составляющей крови.
В случае аллергического отека Квинке механизм развития сходен с анафилактической реакцией. см. Механизм развития анафилаксии
Механизм образования отека
 Отек возникает в глубоких слоях, подкожной жировой клетчатке и слизистых в результате расширения сосудов (венул) и увеличения их проницаемости для жидкой составляющей крови. В результате в тканях накапливается межтканевая жидкость, которая и определяет отек. Расширение сосудов и увеличение их проницаемости происходит в результате выброса биологически активных веществ (брадикинина, гистамина и др.) по описанным выше механизмам (система комплемента, механизм развития анафилаксии).
Отек возникает в глубоких слоях, подкожной жировой клетчатке и слизистых в результате расширения сосудов (венул) и увеличения их проницаемости для жидкой составляющей крови. В результате в тканях накапливается межтканевая жидкость, которая и определяет отек. Расширение сосудов и увеличение их проницаемости происходит в результате выброса биологически активных веществ (брадикинина, гистамина и др.) по описанным выше механизмам (система комплемента, механизм развития анафилаксии).
Стоит отметить, что процесс развития отека Квинке и крапивницы схожи. Только при крапивнице происходит расширение сосудов в поверхностных слоях кожи.
Причины отека Квинке
Основные факторы, провоцирующие проявление наследственного отека Квинке:
- Стресс эмоциональный и физический
- Инфекционные заболевания
- Травма
- Хирургические вмешательства, в том числе и стоматологические манипуляции
- Менструальный цикл
- Беременность
- Прием контрацептивов, содержащих эстрогены
Проявлению приобретенного отека Квинке способствуют следующие заболевания:
- Хронический лимфолейкоз
- Неходжкинская лимфома
- Лимфосаркома
- Миелома
- Первичная криоглобулинемия
- Лимфоцитарная лимфома
- Макроглобулинемия Вальденстрема
Все эти заболевания способствуют снижению уровня ингибитора С1 и повышают возможность неконтролируемой активации комплемента с выбросом биологически активных веществ.
При отеке Квинке связанного с применением ингибиторов АПФ, в основе развития заболевания лежит снижение уровня специфического фермента (ангиотензина II), что в свою очередь приводит к повышению уровня брадикина. И соответственно это ведет к отеку. Ингибиторы АПФ (каптоприл, эналаприл), препараты в основном применяются для контроля артериального давления. Симптомы отека Квинке после употребления таких медикаментов появляются не сразу. В большинстве случаев (70-100%), они проявляются в течение первой недели лечения данными препаратами.
Причины аллергического отека Квинке см. Причины анафилаксии
Виды отека Квинке
Симптомы отека Квинке, фото
Предвестники отека Квинке
Предвестники отека Квинке: покалывание, жжение в области отека. У
35% пациентов розовеет или краснеет кожа туловища или конечностей до или во время отека.
Для того чтобы разобраться с симптомами отека Квинке, нужно понимать, что появление симптомов и их характеристика различна в зависимости от вида отека. Так отек Квинке при анафилактическом шоке или другой аллергической реакции будет отличаться от эпизода наследственного или приобретённого отека Квинке. Рассмотрим симптомы отдельно для каждого вида отека Квинке.
| Вид отека | Симптомы | |||
| Начло и продолжительность отека | Место появления | Характеристика отека | Особенности | |
| Аллергический Отек Квинке | От нескольких минут до часа. Обычно через 5-30 минут. Процесс разрешается через несколько часов или на 2-3 сутки. | Чаще область лица и шеи (губы, веки, щеки), нижние и верхние конечности, половые органы. Отек может возникнуть в любой части тела. | Отек плотный, не образует ямки после надавливания. Отек бледный или слегка красный. | В большинстве случаев сопровождается крапивницей, зудящими высыпаниями. |
| Отек Квинке наследственный и приобретенный, а так же связанный с приемом ингибиторов АПФ, | Отек в большинстве случаев развивается в течение 2-3 часов и исчезает за 2-3 дня, но у некоторых больных может присутствовать до 1 недели. | Отеки чаще появляются в области глаз, губ, языка, половых органов, однако могут проявиться в любой части тела. | Отек чаще бледный, напряженный, отсутствует зуд и покраснение, не остается ямки после надавливания. | Не сопровождается крапивницей. |
| Отек Квинке без найденных причин | См. аллергический отек Квинке | Крапивница возникает в 50% случаев | ||
Симптомы отека Квинке в зависимости от места возникновения
| Место отека | Симптомы | Внешние проявления |
| Отек гортани, языка. | Самое опасное осложнение отека Квинке. Симптомы: нарушение глотание, першение, кашель, нарастающая хрипота, затрудненное дыхание, дыхательная недостаточность. |  |
| Отек в области легких | Выпот жидкости плевральную полость: кашель, боль в груди. |  |
| Отек стенки кишечника | Боли в области живота, рвота, диарея. |  |
| Отек мочевыводящих путей | Задержка мочи |  |
| Отек мозговых оболочек | Головная боль, возможны судороги, нарушение сознания. |  |
Первая неотложная помощь при отеке Квинке

Нужно ли вызывать скорую?
Скорую помощь необходимо вызывать при любом случае отека Квинке. Особенно если это первый эпизод.
Показания к госпитализации:
- Отек языка
- Затрудненное дыхание, вызванное отеком дыхательных путей.
- Отек кишечника (симптомы: боли в области живота, диарея, рвота).
- Отсутствие или незначительный эффект от лечения в домашних условиях.
Чем помочь до приезда скорой помощи?
- Освободить дыхательные пути
- Проверить наличие дыхания
- Проверить пульс и давление
- При необходимости выполнить сердечно-легочную реанимацию. см. Первая помощь при анафилактическом шоке.
- Ввести медикаменты
Тактика медикаментозного лечения при неаллергическом отеке Квинке и при аллергическом немного отличается. Учитывая тот факт, что неаллергический отек Квинке плохо реагирует на основные медикаменты (адреналин, антигистаминные средства, глюкокортикоидные препараты) применяемы для лечения острых аллергических реакций. Однако как показывает практика лучше начать именно с этих медикаментов, особенно если случай отека Квинке впервые выявлен и еще не определена его точная причина.
- Адреналин
- Гормоны
- Антигистаминный препарат
Препараты вводятся в определенной последовательности. В начале, всегда вводится адреналин, затем гормоны и антигистаминные средства. Однако при не столь выраженной аллергической реакции достаточно введение гормонов и антигистаминных средств.
- Адреналин
При первых же симптомах отека Квинке следует ввести адреналин. Это препарат выбора при всех аллергических реакция угрожающих жизни.
Куда вводить адреналин?
Обычно на догоспитальном этапе препарат вводится внутримышечно. Лучшее место для введения адреналина, это средняя треть наружной поверхности бедра. Особенности кровообращения в этой области позволяют препарату быстрее распространиться по организму и начать действовать. Однако адреналин может вводиться и в другие части тела, к примеру, в дельтовидную мышцу плеча, ягодичную мышцу и др. Стоит отметить, что в экстренных ситуациях, когда возникает отек в области шеи, языка, адреналин вводят в трахею или под язык. При необходимости и возможности адреналин вводят внутривенно.
Сколько вводить?
Обычно в таких ситуациях существует стандартная доза для взрослых 0,3-0,5 мл 0,1% раствора адреналина, для детей 0,01 мг/кг веса в среднем 0,1-0,3 мл 0,1% раствора. При отсутствии эффекта введение можно повторять каждые 10-15 минут.
В настоящее время существуют специальные приспособления для удобного введения адреналина, в которых доза строго определена и дозирована. Такими приспособлениями являются шприц-ручка EpiPen, устройство звуковой инструкцией по применению Allerjet. В США и странах Европы, такие устройства носит каждый страдающий анафилактическими реакциями и при необходимости самостоятельно могут произвести себе введение адреналина.
Основные эффекты препарата: Снижает высвобождение веществ аллергической реакции (гистамина, брадикинина и др.), повышает артериальное давление, устраняет спазм в бронхах, повышает эффективность работы сердца.
- Гормональные препараты
Для лечения аллергической реакции применяют следующие препараты: дексаметазон, преднизолон, гидрокортизон.
Куда вводить?
До приезда скорой помощи можно ввести медикаменты внутримышечно, в ту же ягодичную область, но по возможности внутривенно. При отсутствии возможности введения с помощью шприца, возможно содержимое ампулы просто вылить под язык. Под языком находятся вены через препарат хорошо и быстро всасывается. Эффект при введении препарата под язык наступает гораздо быстрее чем при введении внутримышечно даже внутривенно. Так как при попадании лекарственного средства в подъязычные вены оно сразу распространяется, минуя печеночный барьер.
Сколько вводить?
- Дексаметазон от 8-до 32 мг, в одной ампуле 4 мг, 1 таблетка 0,5 мг.
- Преднизолон от 60-150 мг, в одной ампуле 30 мг, 1 таблетка 5 мг.
Медикаменты существуют и в таблетках, однако скорость наступления эффекта гораздо ниже, чем при вышеперечисленных методах введения (в/м и в/в). При необходимости гормоны можно принять в виде таблеток в указанных дозах.
Основные эффекты препаратов: снимают воспаление, отек, зуд, повышают артериальное давление, останавливает высвобождение веществ вызывающих аллергические реакции, способствуют устранению бронхоспазма и улучшению работы сердца.
- Антигистаминные препараты
В основном применяются препараты блокирующие Н1-рецепторы (лоратадин, цетиризин, клемастин, супрастин). Однако доказано, что противоаллергический эффект усиливается при сочетании Н1 и Н2 гистаминблокаторов. К блокаторам Н2- рецепторов относятся: фамотидин, ранитидин и др.
Куда вводить?
Лучше ввести препарат внутримышечно, однако и в виде таблеток препараты будут работать, но с более поздним наступлением эффекта.
Сколько вводить?
Супрастин – 2 мл-2%; в таблетках 50 мг;
Клемастин – 1 мл – 0,1%;
Цетиризин — 20мг;
Лоратадин – 10 мг;
Фамотидин – 20-40 мг;
Ранитидин – 150-300 мг;
Основные эффекты препаратов: устраняют отек, зуд, покраснение, останавливают высвобождение веществ запускающих аллергическую реакцию (гистамина, брадикинина и др.).
Медикаменты, применяемые при неаллергическом отеке Квинкес вязанный с понижением уровня С1-ингибитора (наследственный, приобретенный отек Квинке)
Препараты, которые обычно вводятся при госпитализации:
- Очищенный концентрат С1-ингибитора, вводится внутривенно, применяется в странах Европы и США. В РФ пока не применяется.
- В случае отсутствии концентрата С1-ингибитора. Вводят свежезамороженную плазму 250-300 мл, которая содержит достаточное количество С1-ингибитора. Однако в некоторых случаях её применение может усилить обострение отека Квинке.
Препараты, которые возможно ввести самостоятельно до приезда скорой помощи:
- Аминокапроновая кислота 7-10 г в сутки внутрь д?
