Генетическое заболевание ангионевротический отек лечение
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 7 апреля 2017;
проверки требуют 25 правок.
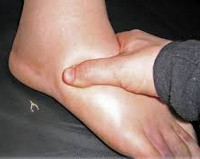
Наследственный ангионевротический отёк (НАО) — редкое заболевание, связанное с количественной недостаточностью (тип НАО — 1) или недостаточной активностью (тип НАО — 2) C1-ингибитора (англ.)русск. системы комплемента человека, что приводит к неконтролируемым внутренним реакциям в крови и проявляется в виде отёков на теле. Чаще всего отеки возникают на руках, ногах, лице, в брюшной полости, а также в гортани.
Отек гортани часто затрудняет поступление воздуха в организм, что в свою очередь, может привести к удушью. Поэтому, в случае возникновения отека гортани, госпитализация обязательна. Отеки в брюшной полости сопровождаются острыми болями и сильной рвотой и также требуют госпитализации.
Патогенез[править | править код]
C1-ингибитор — высокогликозилированный белок сыворотки, синтезируемый в печени и угнетающий протеолитическую активность субкомпонентов Clr и Cls, предупреждая таким образом активацию С4 и С2 компонентов комплемента. Недостаточность C1-ингибитора приводит к неконтролируемой активации ранних компонентов комплемента. Причем в 15 % случаев концентрация С1-ингибитора остаётся в норме, а снижена только его функциональная активность. Определение причины дефицита имеет принципиальное значение для выбора метода лечения этого аутоиммунного заболевания.
Патогенез НАО сходен с патогенезом крапивницы и связан с дилатацией и повышением проницаемости сосудов (преимущественно венул) глубоких (в отличие от крапивницы) слоев дермы и подслизистого слоя, вызванной компонентами комплемента и кининами калликреин-брадикининовой цепи. Кроме того, эти вазоактивные пептиды вызывают спазм гладкой мускулатуры пищеварительного тракта и полых органов.
Типы НАО[править | править код]
Структура C1-ингибитора закодирована в 11-ой хромосоме, этот протеин является альфа-2-глобулином и вырабатывается преимущественно в гепатоцитах, хотя активированные моноциты, мегакариоциты, эндотелиальные клетки и фибробласты способны синтезировать его в небольших количествах. Существуют три типа НАО, фенотипически идентичные.
НАО 1-го типа[править | править код]
НАО 1-го типа (85 % случаев). Дефицит С1-ингибитора обусловлен нефункционирующим геном. Мутация заключается в разнообразных включениях или делециях одного или нескольких нуклеотидов в области гена, кодирующего С1-ингибитор. Мутация наследуется как аутосомно-доминантный, менделирующий признак, хотя приблизительно 25 % случаев НАО обусловлены спонтанной мутацией.
НАО 2-го типа[править | править код]
НАО 2-го типа (15 % случаев). У пациента вырабатывается нормальное или повышенное количество неправильно функционирующего С1-ингибитора. Обычная причина — точечная мутация в позиции Аргинин 444 локуса, который кодирует «реактивный центр» — активный связывающий/разделяющий участок молекулы. Не функционирующий С1-ингибитор не расходуется, что приводит к более высокой, чем в норме, концентрации в сыворотке крови.
НАО 3-го типа[править | править код]
НАО 3-го типа (распространённость неизвестна) — недавно описанное заболевание. Концентрация С1-ингибитора в плазме крови нормальная, механизм заболевания неизвестен и, вероятно, не связан с С1-ингибитором. До недавнего времени считалось, что этот тип НАО встречается только у женщин (характер родословных предполагает Х-сцепленный доминантный тип наследования), однако были выявлены семьи, в которых данный тип НАО был диагностирован и у мужчин.
Приобретенный ангионевротический отёк вследствие дефицита С1-ингибитора встречается у пожилых людей, часто ассоциирован с лимфопролиферативными заболеваниями, наличием антител к С1-ингибитору или с хронической инфекцией.
История НАО[править | править код]
Начало истории наследственного ангиоотека положил немецкий врач-терапевт и хирург, автор большого числа открытий и новшеств в области медицины Иренеус Квинке.
1882 — Иренеус Квинке впервые описывает отёк Квинке.
1888 — У. Осиер (W. Osier) наблюдает и описывает наследственную форму отека Квинке. Отеки периодически появляются у 24-летней женщины. Осиер обращает внимание на семейную форму данного заболевания, так как подобные симптомы наблюдались у пяти предшедствующих поколений семьи пациентки. Отек впервые описывается, как Наследсвенный ангионевротический отек.
1917 — Становится известно об аутосомно-доминантном характере заболевания
1963 — Donaldson и Evans описали причину этого заболевания как биохимический дефект — отсутствие ингибитора С1 (C1INH deficiency).
1986 — Было установлено, что этот генный дефект связан с хромосомой 11.
1972 — Caldwell впервые описал взаимосвязь дефицита ингибитора С1-эстеразы с лимфопролиферативными заболеваниями (приобретённый ангиоотек)
1987 — Alsenz, Bork и Loos обнаружили IgG1-антитела к ингибитору С1-эстеразы (приобретённый ангиоотек).
2000 — описаны эстрогензависимые отеки.
Лечение наследственного ангионевротического отёка[править | править код]
Лечение во время острых приступов наследственного ангионевротического отёка[править | править код]
Лечение должно быть начато настолько рано, насколько это возможно!
- Концентрат C1-ингибитора.
- нативный С1-ингибитор (выделенный из плазмы): Berinert, Cinryze (у подростков и взрослых), Cetor;
- рекомбинантный С1-ингибитор (получаемый из молока генномодифицированных кроликов): Rhucin.
- Антагонисты рецептора к брадикинину: инкатибант (только для взрослых, в педиатрии исследования продолжаются).
- Ингибитор калликреина: Kalbitor (Ecallantide)
- Свежезамороженная плазма, если нет возможности использовать препараты С1-ингибитора и другие современные лекарства.
Долгосрочная профилактика наследственного ангионевротического отёка[править | править код]
Долгосрочная профилактика требуется пациентам, если:
- частота обострений НАО более, чем одно обострение в месяц;
- когда-либо возникал отёк гортани;
- когда-либо требовалась интубация трахеи или госпитализации в отделение реанимации/интенсивной терапии;
- приступы НАО сопровождаются временной нетрудоспособностью или пропусками занятий более, чем 10 дней в год;
- из-за приступов НАО наблюдается значительное снижение качества жизни;
- у пациента существует какая-либо наркотическая зависимость;
- контакт пациента с центрами здравоохранения ограничен;
- у пациента происходит резкое развитие обострений НАО;
- если неэффективна т. н. on-demand therapy (терапия по требованию).
Для долгосрочной профилактики эксперты Международного Консенсуса по лечению НАО (2010) рекомендуют следующие группы препаратов:
- Т. н. «облегчённые» андрогены: Станозолол, Даназол, Оксандролон.
Эта группа препаратов достаточно эффективна, но обладает большим количеством серьёзных побочных эффектов. И, если для получения клинического эффекта (состояния контролируемости) необходима доза более 200мг/сутки (по Даназолу), то следует взвесить ожидаемую пользу и возможный риск развития побочных эффектов. - Ингибиторы фибринолиза (антифибринолитики): ε-аминокапроновая и Транексамовая кислоты.
Эти препараты могут быть эффективны для долгосрочной профилактики, но имеют многочисленные побочные эффекты, в связи с чем специалисты предпочитают назначению этой группы применение андрогенов, как более эффективных средств. - С-1 ингибитор
а) нативный (плазменный): Cinryze (у подростков и взрослых), Berinert, Cetor,
б) рекомбинантный: Rhucin, Ruconest — пока проходит клинические испытания для разрешения использования в качестве профилактического средства). Его эффективность показана в многоцентровых исследованиях.
Краткосрочная профилактика наследственного ангионевротического отёка[править | править код]
Рекомендована всем пациентам с НАО накануне медицинских, стоматологических манипуляций (в том числе и малых), перед действием стрессорных факторов (например, экзамен, собеседование и т. д.).
Применяются препараты, используемые для лечения обострений НАО. В случае наличия симптомов продромального периода (предвестников) может быть эффективной Транексамовая кислота или Даназол в течение 2-3 дней для предотвращения развития обострения.
Лекарственные препараты, применяемые для лечения и профилактики наследственного ангионевротического отёка[править | править код]
В настоящее время для лечения НАО рекомендованы и применяются на практике в различных странах следующие препараты:
- Инкатибант — антагонист рецептора B2 (англ.)русск.. Производитель: Shire Human Genetic Therapies (HGT).
- Berinert — концентрат C1-ингибитора. Производитель: CSL Behring.
- Cinryze — концентрат C1-ингибитора. Производитель: Viropharma.
- Cetor — концентрат C1-ингибитора. Производитель: Sanquin.
- Kalbitor — ингибитор Калликреина — Ecallantide (DX-88). Производитель: Dyax Corp.
- Ruconest — Рекомбинантный C1 ингибитор. Производитель: Swedish Orphan Biovitrum (Sobi).
- Rhucin — Рекомбинантный C1 ингибитор. Производитель: Pharming Group NV.
- Станозолол — анаболический стероидный препарат, производное андростана (дигидротестостерона). Торговые наименования: Winstrol (пероральный), Tenabol и Winstrol Depot (внутримышечный).
- Даназол — антигонадотропное средство, являющееся синтетическим андрогеном, полученным из этистерона. Торговые наименования: Даназол, Дановал, Данол, Danocrine.
- Оксандролон — анаболический стероидный препарат, получаемый на основе дигидротестостерона. Торговые наименования: Oxandrin, Anavar
- Транексамовая кислота — антифибринолитическое, противоаллергическое, противовоспалительное вещество. Торговые наименования: Транексам, Транексамовая кислота, Трансамча, Троксаминат, Экзацил
- Аминокапроновая кислота — лекарственное гемостатическое средство. Торговые наименования: Amicar, Поликапран (Polycapran), ε-Ahx, 6-aminohexanoic acid.
Лекарственные препараты, которых следует избегать при наследственном ангионевротическом отёке[править | править код]
Препараты этих типов могут провоцировать приступы НАО:
- Ингибиторы АПФ
- Эстрогенсодержащие контрацептивы
- Заместительная гормональная терапия
Международная организация пациентов НАО[править | править код]
В ноябре 2004 года, во Франции была зарегистрирована международная организация пациентов с недостаточностью C1-ингибитора HAEi[1].
Организация оказывает помощь специалистам НАО, а также национальным организациям и группам пациентов НАО по всему миру. Целью международной организации пациентов НАО является облегчение доступа к эффективной диагностике и лечению Наследственного ангионевротического отёка (отёка Квинке и других заболеваний, связанных с дефицитом ингибитора C1).
«Общество пациентов с Наследственным Ангионевротическим Отеком». (МОО «ОПНАО»).[править | править код]
В мае 2016 года, в России была зарегистрирована межрегиональная общественная организация «Общество пациентов с Наследственным Ангионевротическим Отеком».
Целью организации является объединение членов для объединения и консолидации пациентов с Наследственным Ангионевротическим Отеком, содействия в решении проблем лечения и профилактики заболевания, реабилитационного и санаторного лечения, предупреждения и снижения инвалидности, в том числе детей и подростков, страдающих Наследственным Ангионевротическим Отеком, содействия в организации получения ими необходимого образования, трудоустройства и социально-бытового обеспечения с учётом специфики заболевания.[2]
День НАО[править | править код]
16 мая — ежегодный международный день осведомленности о НАО. Мероприятия, приуроченные ко дню НАО и проводимые по всему миру, направлены на повышение знаний о заболевании в обществе и среди специалистов, ранней и более точной диагностике, эффективному лечению и профилактике — всему тому, что позволит пациентам НАО вести нормальный образ жизни. Дню НАО посвящён веб-сайт www.haeday.org.
Примечания[править | править код]
Ссылки[править | править код]
- www.hereditary-angioedema.org — Наследственный/врождённый ангиоотек (НАО), Hereditary Angioedema (HAE), Наследственный ангионевротический отек (НАО)
- www.haei.org — HAEI — International Patient Organization for C1-Inhibitor Deficiencies
- www.haeday.org — hae day 🙂
- https://facebook.com/groups/HAEinternational — международное facebook-сообщество « HAEI — International Patient Organization for C1 Inhibitor Deficiencies»
- www.allabouthae.com — американское сообщество врачей и пациентов НАО. На сайте можно проверить симптомы, составить генетическое дерево, задать вопрос специалисту, создать и вести свой дневник, делиться личными историями о болезни с другими пользователями сайта.
- www.haea.org — американское сообщество врачей и пациентов НАО. На сайте есть фотографии отеков (до и во время).
- www.immuno.health-ua.com/article/40.html — Наследственный ангионевротический отек — статья Л. В. Забродской
- www.op-nao.ru — Российская Межрегиональная общественная организация «Общество пациентов с Наследственным Ангионевротическим Отеком». (МОО «ОПНАО»).
- by.haei.org — Республиканское общественное объединение “Помощь пациентам НАО” (Беларусь)
Источник
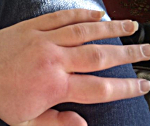
Наследственный ангионевротический отек – генетическое заболевание, при котором наблюдается дефицит ингибитора С1-компонента комплемента. Симптомами являются рецидивирующие отеки кожи, слизистых оболочек и органов брюшной полости, которые могут сопровождаться удушьем (при отеке гортани), рвотой и болями в животе (при поражении брюшной полости). Диагностика производится на основании осмотра, изучения наследственного анамнеза, определения С1-ингибитора, компонентов С4 и С2 в плазме крови, молекулярно-генетических исследований. Лечение осуществляется путем компенсирования абсолютного или функционального дефицита С1-ингибитора, применения блокаторов брадикинина и калликреина, использования свежезамороженной донорской плазмы.
Общие сведения
Наследственный ангионевротический отек (НАО) – вариант первичного иммунодефицита, обусловленный нарушением ингибирования системы комплемента, точнее, его основной фракции С1. Впервые это состояние было описано в 1888 году У. Осиером, который выявил рецидивирующие отеки у молодой женщины, а также установил, что подобное заболевание имелось как минимум у пяти поколений ее семьи. Примечательно, что собственно ангионевротический отек был открыт И. Квинке всего за 6 лет до обнаружения наследственной формы этой патологии – в 1882-м году. Наследственный ангионевротический отек имеет аутосомно-доминантный характер передачи и с одинаковой частотой поражает как мужчин, так и женщин. По некоторым данным, у женщин заболевание протекает тяжелее и возникает раньше, однако достоверных исследований по этому поводу не производилось. Встречаемость наследственного ангионевротического отека, по всей видимости, значительно варьирует у разных этнических групп, что дает весьма неоднородные цифры этого показателя – от 1:10 000 до 1:200 000.

Наследственный ангионевротический отек
Причины наследственного ангионевротического отека
Непосредственной причиной развития наследственного ангионевротического отека является первичный иммунодефицит, заключающийся в дефиците или функциональной неполноценности ингибитора эстеразы одного из компонентов комплемента – С1. В результате этого также нарушается ингибирование активации других компонентов этой системы – С4 и С2, что приводит к еще большему расстройству работы данного иммунного механизма. Врачам-генетикам удалось установить ген, отвечающий за 98% форм наследственного ангионевротического отека – им является C1NH, расположенный на 11-й хромосоме и кодирующий вышеуказанный ингибитор эстеразы С1. Различные мутации способны приводить к неодинаковым по своему течению формам заболевания, которые обладают достаточно сходными клиническими проявлениями, но различаются при проведении ряда диагностических тестов.
При одних типах мутации гена C1NH происходит полное прекращение синтеза белка-ингибитора С1, в результате чего он отсутствует в плазме крови, а остановка системы комплемента производится малоэффективными побочными путями. В других случаях наследственный ангионевротический отек возникает на фоне нормального содержания ингибитора в крови, при этом генетический дефект C1NH приводит к нарушению структуры активного центра данного фермента. В результате ингибитор С1 становится функционально неполноценным, что и служит причиной развития патологии. Существуют также редкие формы наследственного ангионевротического отека, при которых не наблюдается как изменений количества или активности ингибитора эстеразы С1, так и мутаций в гене C1NH – этиология и патогенез таких заболеваний на сегодняшний день неизвестны.
Остановка ингибирования активности компонентов комплемента (С1, С2, С4) приводит к запуску иммунной реакции, сходной по своему течению с аллергической, особенно крапивницей. Компоненты комплемента способны расширять кровеносные сосуды глубоких слоев дермы, повышать проницаемость их стенок, что провоцирует диффундирование компонентов плазмы крови в межклеточное пространство тканей кожи и слизистых оболочек и приводит к их отеку. Кроме того, немаловажную роль в патогенезе наследственного ангионевротического отека играют вазоактивные полипептиды – брадикинин и калликреин, которые еще больше увеличивают степень отека, а также способны вызывать спазм гладкомышечной мускулатуры органов желудочно-кишечного тракта. Эти процессы обуславливают все разнообразие симптомов наследственного ангионевротического отека: отечность кожи (в области конечностей, лица, шеи) и слизистых оболочек (ротовой полости, гортани, глотки), боли в животе и диспепсические расстройства, провоцируемые сочетанием отеков и спазмов.
Классификация наследственного ангионевротического отека
Всего на сегодняшний день выявлено три основных типа наследственного ангионевротического отека. Их различия в плане клинического течения патологии очень незначительны, для определения формы заболевания используют специальные диагностические методики. Врачу-иммунологу крайне важно выяснить тип наследственного ангионевротического отека, так как от этого во многом зависит тактика лечения данной патологии:
- Наследственный ангионевротический отек 1-го типа (НАО-1) – является наиболее распространенной формой заболевания, регистрируется у 80-85% больных с такой патологией. Причиной НАО этого типа является отсутствие гена C1NH или нонсенс-мутация в нем, в результате чего ингибитор С1 не образуется в организме.
- Наследственный ангионевротический отек 2-го типа (НАО-2) – более редкая форма патологии, выявляется лишь у 15% больных. Обусловлен также генетическим дефектом в C1NH, однако при этом экспрессия белка-ингибитора С1 не останавливается, а сам фермент имеет измененную структуру своего активного центра. Это приводит к его неполноценности, и он становится неспособен правильно выполнять свои функции.
- Наследственный ангионевротический отек 3-го типа – относительно недавно обнаруженная форма заболевания с практически неизученными этиологией и патогенезом. Достоверно удалось выяснить, что при этом типе отека отсутствуют мутации гена C1NH, сохраняется нормальное количество ингибитора эстеразы компонента комплемента С1 и его функциональная активность. Больше никаких данных по поводу данной формы (или их совокупности) наследственного ангионевротического отека не имеется.
Симптомы наследственного ангионевротического отека
Как правило, при рождении и в детском возрасте (за исключением редких случаев) наследственный ангионевротический отек ничем себя не проявляет. Довольно часто первые признаки заболевания возникают в подростковом периоде, так как их провоцируют стрессы и гормональные перестройки, происходящие в организме в это время. Однако нередко наследственный ангионевротический отек появляется позже – в возрасте 20-30 лет или даже у пожилых лиц. Чаще всего развитию первого приступа предшествует какое-либо провоцирующее явление: мощный эмоциональный стресс, серьезное заболевание, хирургическое вмешательство, прием некоторых лекарственных средств. В дальнейшем «порог чувствительности» по отношению к провоцирующим факторам снижается, приступы возникают все чаще – наследственный ангионевротический отек приобретает рецидивирующий характер.
Основным проявлением заболевания у большинства больных является отек кожи и подкожной клетчатки на кистях, стопах, иногда лице и шее. В более тяжелых случаях отечные явления возникают на слизистых оболочках полости рта, гортани и глотки – при этом может развиваться удушье (асфиксия), являющееся наиболее частой причиной смерти от наследственного ангионевротического отека. В других случаях на первый план выступают симптомы со стороны желудочно-кишечного тракта: тошнота, рвота, боли и рези в животе, иногда подобная клиническая картина приобретает черты «острого живота». В отдельных случаях наследственный ангионевротический отек характеризуется сочетанием отека кожи, слизистых оболочек и поражения желудочно-кишечного тракта.
Диагностика наследственного ангионевротического отека
Для выявления наследственного ангионевротического отека используют данные физикального осмотра больного, изучения его наследственного анамнеза, определения в крови количества ингибитора С1, а также компонентов комплемента С1, С2, С4, и молекулярно-генетических исследований. Осмотр в фазу обострения заболевания выявляет отек кожи или слизистых оболочек, пациенты могут жаловаться на боли в животе, рвоту, диарею. В крови при наличии наследственного ангионевротического отека 1-го типа ингибитор эстеразы С1 полностью отсутствует, значительно снижены концентрации индикаторных компонентов комплемента. При 2-м типе заболевания в плазме крове может определяться незначительное количество ингибитора С1, в редких случаях его уровень соответствует норме, но соединение имеет пониженную функциональную активность. При всех трех вариантах наследственного ангионевротического отека уровень С1, С2 и С4 не превышает 30-40% от нормы, поэтому этот показатель является ключевым в диагностике данного состояния.
Изучение наследственного анамнеза пациента зачастую обнаруживает наличие подобного заболевания как минимум у нескольких поколений его предков и у других родственников. Однако отсутствие признаков семейного характера патологии не является однозначным критерием, позволяющим исключить наследственный ангионевротический отек – примерно у четверти больных это состояние обусловлено спонтанными мутациями и выявляется впервые в семье. Молекулярно-генетическая диагностика осуществляется путем автоматического секвенирования гена C1NH с целью выявления мутаций. Дифференциальную диагностику следует производить с ангионевротическим отеком аллергического генеза и приобретенными формами дефицита ингибитора С1.
Лечение наследственного ангионевротического отека
Терапию наследственного ангионевротического отека разделяют на два типа – лечение для купирования острого приступа заболевания и профилактический прием препаратов для предупреждения их развития. В случае острого отека Квинке, обусловленного НАО, традиционные противоанафилактические меры (адреналин, стероиды) неэффективны, необходимо использовать нативный или рекомбинантный ингибитор С1, антагонисты брадикинина и калликреина, при их отсутствии показано переливание свежезамороженной плазмы. Начинать такое лечение нужно как можно раньше, в идеале – при самых первых приступах наследственного ангионевротического отека.
Долгосрочная профилактика заболевания производится в тех случаях, когда приступы возникают слишком часто (чаще раза в месяц), если в анамнезе имелись случаи отека гортани или удушья, либо госпитализация в реанимационное отделение. Профилактика включает в себя использование андрогенов, экзогенных (рекомбинантных или нативных) форм ингибитора эстеразы С1, антифибринолитических препаратов. При доброкачественном течении наследственного ангионевротического отека – редких приступах и их относительно быстром исчезновении – такое лечение может не назначаться. Однако накануне хирургических или стоматологических вмешательств, физических и умственных нагрузок рекомендуется краткосрочно принимать вышеуказанные средства для уменьшения риска развития приступа.
Прогноз и профилактика наследственного ангионевротического отека
В большинстве случаев прогноз наследственного ангионевротического отека относительно благоприятный в плане выживаемости – при разумном лечении и профилактике приступы возникают крайне редко и не угрожают жизни больного. При этом всегда сохраняется риск отека гортани, что может привести к асфиксии и летальному исходу. Таким больным следует не только избегать значительных физических и эмоциональных нагрузок, но и желательно иметь при себе карточку или медальон с указанием диагноза. Огромное количество смертей от наследственного ангионевротического отека было обусловлено неверными действиями медиков, не знающих диагноза и поэтому использующих традиционные при аллергическом отеке Квинке препараты, которые неэффективны при НАО.
Источник
